
用H2O2和H2SO4的混合溶液可溶出废旧印刷电路板上的铜.已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H1=+64.39kJ/mol2H2O2(l)═2H2O(l)+O2(g)△H2=﹣196.46kJ/molH2(g)+ O2(g)═H2O(l)△H3=﹣285.84kJ/mol求在H2SO4溶液中,Cu与H2O2反应生成Cu2+(aq)和H2O(l)的反应热为多少?
O2(g)═H2O(l)△H3=﹣285.84kJ/mol求在H2SO4溶液中,Cu与H2O2反应生成Cu2+(aq)和H2O(l)的反应热为多少?
考点: 有关反应热的计算.
专题: 化学反应中的能量变化.
分析: 根据已知的热化学反应方程式和盖斯定律来分析Cu与H2O2反应生成Cu2+和H2O的热化学方程式,由盖斯定律①+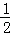 ×②+③得到:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H,由盖斯定律可知该反应的反应热△H=H1+H2×
×②+③得到:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H,由盖斯定律可知该反应的反应热△H=H1+H2×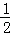 +H3,据此分析解答.
+H3,据此分析解答.
解答: 解:①Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64.39kJ/mol,
②2H2O2(l)═2H2O(l)+O2(g)△H=﹣196.46kJ/mol,
③H2(g)+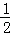 O2(g)═H2O(l)△H=﹣285.84kJ/mol,
O2(g)═H2O(l)△H=﹣285.84kJ/mol,
由盖斯定律①+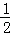 ×②+③得到:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=+64.39kJ/mol+
×②+③得到:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=+64.39kJ/mol+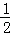 ×(﹣196.46kJ/mol)+(﹣285.84kJ/mol)=﹣319.68kJ/mol,
×(﹣196.46kJ/mol)+(﹣285.84kJ/mol)=﹣319.68kJ/mol,
答:Cu与H2O2反应生成Cu2+(aq)和H2O(l)的反应热为:﹣319.68kJ/mol;
点评: 本题考查反应热的有关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,明确反应热和化学计量数的关系是解题关键,题目难度不大.注意盖斯定律的应用.


科目:高中化学 来源: 题型:
现有下列物质:①KI ②铜 ③稀硝酸 ④NH3 ⑤NaHSO4  ⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水
⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水
(1)按物质的分类方法填写表格的空白处(填物质编号)
分类标准 电解质 盐 非电解质 混合物
属于该类的物质
(2)上述某两种物质在溶液中可发生离子反应:H++OH﹣═H2O,写出该离子反应对应的化学方程式 .
(3)物质①的稀溶液在空气中被氧化,加入淀粉溶液显蓝色,则反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在固定体积的密闭容器中发生下列反应:2HI(g)⇌H2(g)+I2(g).若c(HI)由0.1mol/L 降到0.07mol/L时,需要15s,那么c(HI)由0.07mol/L 降到0.05mol/L时,所需反应的时间为()
A. 等于5 s B. 等于10 s C. 大于10 s D. 小于10 s
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. 升高温度能使化学反应速率增大,主要原因是增加了反应物分子 中活化分子的百分数
中活化分子的百分数
B. 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C. 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大
D. 催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,浓度都是1mol•L﹣1的两种气体X2和Y2,在密闭容器中反应生成气体Z,经过t min后,测得物质的浓度分别为c(X2)=0.6mol•L﹣1,c(Y2)=0.8mol•L﹣1,c(Z)=0.4mol•L﹣1,则该反应的反应式可表示为()
A. X2+2Y2═2XY2 B. 2X2+Y2═2X2Y C. 3X2+Y2═2X3Y D. X2+3Y2═2XY3
查看答案和解析>>
科目:高中化学 来源: 题型:
火电厂利用燃煤发电,煤燃烧中的热化学方程式有:C(s)+O2(g)═CO2(g)△H1=﹣393.5kJ/molCO(g)+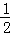 O2(g)═CO2(g)△H2=﹣283kJ/mol C(s)+
O2(g)═CO2(g)△H2=﹣283kJ/mol C(s)+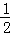 O2(g)═CO(g)△H3=?下列有关说法中不正确的是()
O2(g)═CO(g)△H3=?下列有关说法中不正确的是()
A. CO的燃烧热为283 kJ/mol
B. 二氧化碳分解为一氧化碳和氧气的反应是吸热反应
C. △H3=△H2﹣△H1=110.5 kJ/mol
D. △H3=△H1﹣△H2=﹣110.5 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
热化学方程式C(s)+H2O(g) CO(g)+H2(g);△H=+131.3kJ/mol表示()
CO(g)+H2(g);△H=+131.3kJ/mol表示()
A. 碳和水反应吸收131.3kJ能量
B. 1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C. 1mol固态碳和1mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ
D. 1个固态碳原子和1分子水蒸气反应吸热131.1kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃、101kPa下,如图所示,石墨的燃烧热为393.5kJ/
mol,金刚石的燃烧热为395.0kJ/mol.下列说法或表达正确的是
()
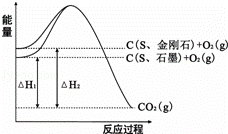
A. 金刚石比石墨稳定
B. C(s、石墨)=C(s、金刚石)△H=+1.5kJ/mol
C. △H1<△H2
D. 如果使用催化剂,△H1和△H2都变小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com