
下列粒子的结构示意图中,表示氯离子的是
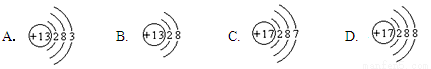
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源:2014-2015学年湖南省高二上学期期中化学(理)试卷(解析版) 题型:选择题
对已经达到化学平衡的反应:COCl2(g)  CO(g) + Cl2(g),△H>0 当反应达到平衡时下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减小压强 ⑤加催化剂,其中能提高COCl2(g)转化率的是
CO(g) + Cl2(g),△H>0 当反应达到平衡时下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减小压强 ⑤加催化剂,其中能提高COCl2(g)转化率的是
A.①⑤ B.①④ C.②③ D.③⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省伊春市高二上学期期中化学试卷(解析版) 题型:选择题
对于达到平衡的可逆反应:X+Y W+Z,其他条件不变时,增大压强,正、逆反应速率变化的情况如图所示。
W+Z,其他条件不变时,增大压强,正、逆反应速率变化的情况如图所示。

下列对X、Y、W、Z四种物质状态的描述正确的是
A.W、Z均为气体,X、Y中只有一种为气体
B.X、Y均为气体,W、Z中只有一种为气体
C.X、Y或W、Z中均只有一种为气体
D.X、Y均为气体,W、Z均为液体或固体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中化学(文)试卷(解析版) 题型:实验题
某中学化学研究性学习小组利用以下装置制取并探究氨气的性质。A中发生反应的化学方程式: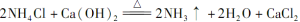
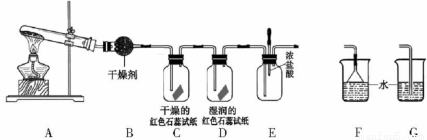
【实验探究】
(1)A中的反应 (填“是”或“不是”)氧化还原反应。
(2)A装置还可用于制取气体 (只填一种)
(3)若有10.7gNH4Cl固体,最多可制取NH3(标准状况)的体积是 L (NH4C1的摩尔质量为53.5g·mol-1)。
(4)实验室收集氨气的方法是
(5)C、D装置中颜色会发生变化的是 (填“C”或“D”)
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴人1-2滴浓盐酸,可观察到的现象是
(7)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是 (填“F”或“G”)。
【知识拓展】
(8)生石灰与水反应生成Ca(OH)2并放出热量[化学方程式为CaO+H2O==Ca(OH)2]。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。你认为生石灰可用下列 物质代替(填序号)。
A.碱石灰(NaOH与CaO的固体混合物) B.NaOH 固体
C.硫酸溶液 D.石灰石(含CaCO3)
【知识应用】
(9)2010年11月9日晚,我省宁德市一冷冻厂发生氨气泄漏事件,500 多居民深夜大转移。假如你在现场,你会采用什么自救为法?
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中化学(文)试卷(解析版) 题型:选择题
下列有关物质用途的说法中,不正确的是
A.硝酸可用于制氮肥 B.氯气可用于制漂白粉
C.硅可用于制光导纤维 D.硅酸钠可用于制木材防火剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中化学(理)试卷(解析版) 题型:填空题
(12分)氨是最重要的氮肥,是产量最大的化工产品之一。德国人哈伯在1905年发明了合成氨的方法,其合成原理为:N2(g)+3H2(g)  2NH3(g) ΔH= -92.4 kJ·mol-1,他因此获得了1918年诺贝尔化学奖。在密闭容器中,使2 mol N2和6 mol H2混合发生上述反应,达到平衡:
2NH3(g) ΔH= -92.4 kJ·mol-1,他因此获得了1918年诺贝尔化学奖。在密闭容器中,使2 mol N2和6 mol H2混合发生上述反应,达到平衡:
(1)此时,N2和H2的浓度比是 ;N2和H2的转化率比是 。
(2)若恒容下升高温度,则混合气体的相对分子质量 ;密度 。(填“变大”“变小”或“不变”)。
(3)若充入氩气,并保持压强不变,平衡将 ;(填“正向”“逆向”或“不”)移动。
(4)若容器恒容、绝热, 加热使容器内温度迅速升至原来的2倍,达到新平衡后,容器内温度 (填“大于”“小于”或“等于”)原来的2倍。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中化学(理)试卷(解析版) 题型:选择题
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为在硬币制作时,钢芯应做
A.正极 B.负极 C.阴极 D.阳极
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三上学期期中化学试卷(解析版) 题型:选择题
用NA表示阿佛加德罗常数,下列说法正确的是
A.300 mL 2 mol·L-1的蔗糖溶液中所含分子数为0.6NA
B.在标准状况下,2.8g N2和2.8g CO所含电子数不相等
C.0.2 mol H2O2完全分解转移的电子数为0.2NA
D.在常温常压下,2.24L SO2与O2的混合气体中所含氧原子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com