
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源:不详 题型:单选题
| A.稳定性:H2X H2Z | B.酸性:H2ZO3<H2ZO4 |
| C.还原性:W-<Z2- | D.半径:Y3+<Z2- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.以铝为阳极、铜为阴极电解硫酸铜溶液时,阳极铝溶解 |
| B.与氯气反应时,铝失去3个电子,而铜失去2个电子 |
| C.常温下,铝在浓硝酸中钝化而铜不发生钝化 |
| D.常温下将铝和铜用导线连接放入到稀盐酸中,铝为负极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稳定性:NH3<PH3<SiH4 | B.酸性:HClO4>H2SO4>H3PO4 |
| C.碱性:KOH>NaOH>Mg(OH)2 | D.还原性:F-<Cl-<Br- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
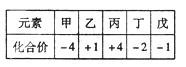
| A.乙的单质中能与水剧烈反应 |
| B.气态氢化物的稳定性:丙>甲 |
| C.丙的氧化物能与戊的氢化物水溶液反应 |
| D.其最高价氧化物对应的水化物的酸性:丁>戊 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素 | 相关信息 |
| X | 啤酒和饮料中常溶有X的最高价氧化物,打开瓶子时,这种氧化物会大量逸出 |
| Y | Y2是空气中含量最高的气体单质 |
| Z | Z的基态原子最外层电子排布式为2s22p4 |
| W | W的一种核素质量数为27,中子数为14 |
 Y2O4(g) △H2=-56.9kJ/mol
Y2O4(g) △H2=-56.9kJ/mol查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | | R | | |
| T | Q | | W | K |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| X | X是地壳中含量最多的元素 |
| Y | Y元素原子核外3p能级上有4个电子 |
| Z | 核素Z的质量数为14、中子数为7 |
| T | T的单质是一种常见的金属,其新制的氢氧化物悬浊液可用于检验糖尿病 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
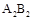
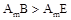
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com