
下图是一种正在投入生产的大型蓄电系统。左右两侧为电解质储罐,中央为电池,利用2Na2S2+NaBr3 Na2S4+3NaBr反应原理进行工作,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过。
Na2S4+3NaBr反应原理进行工作,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过。
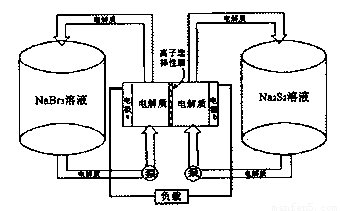
(1)当蓄电池工作放电时,电池中Na+的移动方向是:____ (填“电极a→b”或“电极b→a”),电极a的电极名称为 ,发生的电极反应为 。
(2)当蓄电池处于充电状态时,电极a应接外电源 极(填“正”或“负”),电极b的电极名称为 ,发生的电极反应为 。
(3)若左侧储罐的中溶液体积为VL(导管、泵及电池内部溶液忽略不计),一段时间观察,溶液中Na+的平均浓度由c1mol·L-1降至c2mol·L-1,则此装置该段时间正处于 (填“放电”或“充电”)状态,此过程中电极b上转移电子的物质的量共有__ mol。
(1)电极b→a (2分) 正极(1分) Br— 3+2e-=3Br-(2分)
(2)正(2分) 阴极(2分) S2— 4+2e-=2S2— 2(2分) (3)充电(2分) (c1—c2)V(2分)
【解析】
试题分析:(1)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。根据总的反应方程式可知,Na2S2失去电子,被氧化,所以b电极是负极,因此当蓄电池工作放电时,电池中Na+的移动方向是电极b→a。电极a的电极名称为是正极,发生还原反应,因此电极反应式是Br— 3+2e-=3Br-。
(2)电极a是正极,因此当蓄电池处于充电状态时,电极a应接外电源正极。电极b与外接电源的负极相连,作阴极,得到电子,发生还原反应,因此此时电极反应式是S2— 4+2e-=2S2— 2。
(3)放电时钠离子向左侧移动,因此当左侧钠离子浓度降低时,说明处于充电状态。钠离子带1个正电荷,所以根据电荷守恒可知,此过程中电极b上转移电子的物质的量共有(c1—c2)mol/L×VL=(c1—c2)V。
考点:考查电化学原理应用的有关判断


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:

| 放电 |
| 充电 |
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
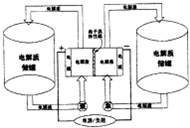 下图是一种正在投入生产的大型蓄电系统.左右两侧为电解质储罐,中央为电池,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;放电前,被膜隔开的电解质为Na2S2和NaIX(3≤x≤5),放电后,分别变为Na2S4和NaI.则下列说法不正确的是( )
下图是一种正在投入生产的大型蓄电系统.左右两侧为电解质储罐,中央为电池,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;放电前,被膜隔开的电解质为Na2S2和NaIX(3≤x≤5),放电后,分别变为Na2S4和NaI.则下列说法不正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
A.充电的过程中当0.1 mol Na+通过离子交换膜时,导线通过0.1 mol电子
B.电池放电时,负极反应为:3NaBr-2e-====NaBr3+2Na+
C.充电过程中钠离子从右到左通过离子交换膜
D.放电过程中钠离子从右到左通过离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
(9分)由硫可制得多硫化钠Na2Sx,x的值一般为2~6。当x=2时,多硫化钠称为过硫化钠。
Ⅰ.过硫化钠加入盐酸中有硫沉淀析出,写出该反应的化学方程式 ,该反应的还原产物是 。
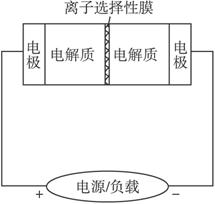
Ⅱ.某些多硫化钠可用于制作蓄电池。下图是一种正在投入生产的大型蓄电系统的原理图。
电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过。电池充、放电的化学反应方程式为:
![]()
(1)电池中的左侧“电极”的电极名称是 (填“正极”或“负极”)。
(2)放电过程中钠离子从 (选“左到右”或“右到左”)通过离子交换膜。
(3)写出充电过程中阳极的电极反应式 。
查看答案和解析>>
科目:高中化学 来源:2010年海南省海口市高三下学期高考调研(一)化学试题 题型:填空题
(9分)由硫可制得多硫化钠Na2Sx,x的值一般为2~6。当x=2时,多硫化钠称为过硫化钠。
Ⅰ.过硫化钠加入盐酸中有硫沉淀析出,写出该反应的化学方程式 ,该反应的还原产物是 。
Ⅱ.某些多硫化钠可用于制作蓄电池。下图是一种正在投入生产的大型蓄电系统的原理图。
电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过。电池充、放电的化学反应方程式为:



(1)电池中的左侧“电极”的电极名称是 (填“正极”或“负极”)。
(2)放电过程中钠离子从 (选“左到右”或“右到左”)通过离子交换膜。
(3)写出充电过程中阳极的电极反应式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com