
| A. |  | B. |  | C. |  | D. |  |
分析 A、氮气分子中存在氮氮三键,氮原子最外层为8电子;
B、CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子;
C、氯离子最外层得到一个电子,达到了最外层8个电子的稳定结构,为阴离子,需要标明所带电荷数;
D、H原子最外层只有一个电子.
解答 解:A、氮气中存在三对共价键,正确应为: ,故A错误;
,故A错误;
B、CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ,故B错误;
,故B错误;
C、氯离子最外层为8个电子,带一个单位的负电荷,正确为: ,故C正确;
,故C正确;
D、H原子最外层只有一个电子,正确应为 ,故D错误,故选C.
,故D错误,故选C.
点评 本题考查的是化学用语,化学用语主要包括元素符号、化学式、化合价、电子式、原子结构示意图、结构式、结构简式以及方程式和各种模型等,需要学生熟练记住.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
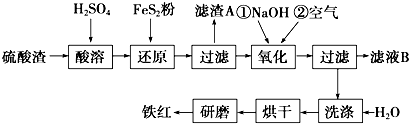
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{6}^{12}C$和${\;}_{6}^{13}C$ | B. | CH3CH2CH2CH3和CH3CH(CH3)2 | ||
| C. | 红磷和白磷 | D. | 冰和干冰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 种 | B. | 2 种 | C. | 3 种 | D. | 4 种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{3}{8}$ mol | B. | $\frac{3}{2}$ mol | C. | 2 mol | D. | 0.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com