
����Ŀ�����̿���Ҫ�ɷ���MnO2����Ũ�����ϼ��ȣ�������������ijѧ��ʹ����һԭ�������ͼ��ʾ��ʵ��װ�ã����������Ƶõ������볱ʪ����ʯ�ҷ�Ӧ��ȡ����Ư�ۣ�����һ�����ȷ�Ӧ�����ݴ˻ش��������⣺

��1��A������������__________
��2��Ư�۽���U�ι��в������仯ѧ����ʽ��____________________��
��3����ʵ��������Ca(ClO)2����̫�ͣ����������������Ϸ��֣���Ҫԭ������U�ι��д�����������Ӧ��
���¶Ƚϸ�ʱ��������ʯ�ҷ�Ӧ����Ca(ClO3)2��Ϊ����˸���Ӧ�ķ������ɲ�ȡ�Ĵ�ʩ��______________________________��
�����ж���һ������Ӧ��д���˷�Ӧ����ʽ����____________________��
��4��Ư�۾�ͬ�������ò���������Ca(ClO)2+4HCl=2Cl2��+CaCl2+2H2O���÷�Ӧ��ÿ����1molCl2��ת�Ƶ��ӵ����ʵ���Ϊ__________mol��
��5����Ч����Ư�۾�����ЧCa(ClO)2�ĺ�����С�ı�־����֪����Ч��=��Ư�۾����������ͷų�������������/Ư�۾���������![]() 100%����Ư�۾�����Ч��Ϊ65%�����Ư�۾���Ca(ClO)2����������Ϊ__________������һλС����
100%����Ư�۾�����Ч��Ϊ65%�����Ư�۾���Ca(ClO)2����������Ϊ__________������һλС����
���𰸡� ��Һ©�� ![]() ��U�ι�������ˮԡ��
��U�ι�������ˮԡ�� ![]() 1 65.5%
1 65.5%
����������1����ͼ֪A�����������Ƿ�Һ©����
��2����������ʯ�ҷ�Ӧ���õ�Ư�۴�����ơ��Ȼ��ƺ�ˮ����U�ι��в����仯ѧ����ʽΪ2Cl2��2Ca(OH)2=CaCl2��Ca(ClO)2��2H2O��
��3�����¶Ƚϸ�ʱ��������ʯ��������Ӧ���ɸ�����Ca(ClO3)2������Ϊ��ֹ����������ɣ�Ӧ���ͷ�Ӧ���¶ȣ���˿��Խ�U�ι�������ˮԡ�С�
����Ϊ�����ӷ�����������ȡ�������л���HCl�����Ȼ�����Ժ���ʯ�ҷ�Ӧ�����Ȼ��ƺ�ˮ���˷�Ӧ����ʽ![]() ��
��
��4���ɷ�Ӧ֪Ca(ClO)2���ȵĻ��ϼ��ǣ�1�ۣ��ڷ�Ӧ�л��ϼ��ɣ�1�۽��͵�0�ۣ����Ca(ClO)2����������ת��2�����ӡ��Ȼ����ǻ�ԭ���������������Ȼ���ֻ��2mol�����Է�Ӧ��ÿ����1mol��������ת��1mol���ӣ����������Ȼ���Ҳ��1mol��
��5����֪����Ч��=��Ư�۾����������ͷų�������������/Ư�۾���������![]() 100%�������������Ʒ�Ӧ��������������ʽ��Ca(ClO)2+4HCl=2Cl2��+CaCl2+2H2O
100%�������������Ʒ�Ӧ��������������ʽ��Ca(ClO)2+4HCl=2Cl2��+CaCl2+2H2O
143 2![]() 71
71
x y
y=71![]() 2x/143
2x/143![]() 100%,��ΪƯ�۾�����Ч��Ϊ65%������71
100%,��ΪƯ�۾�����Ч��Ϊ65%������71![]() 2x/143
2x/143![]() 100%=65%
100%=65%
X= 65.5%,��ˣ�������ȷ���ǣ�65.5%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NH3��H2S���Ǽ��Է��ӣ�CO2��BF3��CCl4���Ǻ����Լ��ķǼ��Է��ӡ���������ʵ�����Ƴ�ABn�ͷ����ǷǼ��Է��ӵľ��������(����)
A. �����в��ܺ�����ԭ��
B. ��ABn������A�����ԭ������ӦС��B�����ԭ������
C. ��ABn������Aԭ��û�йµ��Ӷ�
D. ������ÿ�����ۼ��ļ���Ӧ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ��ǿ������������������������ȡ�
��1��O3��KI��Һ��Ӧ���ɵ����ֵ�����___________��_________�������ʽ����
��2��O3��ˮ���ֽ⣬һ�������£�O3��Ũ�ȼ���һ�������ʱ�䣨t�������ʾ����֪��O3����ʼŨ��Ϊ0.0216 mol/L��
| 3.0 | 4.0 | 5.0 | 6.0 |
20 | 301 | 231 | 169 | 58 |
30 | 158 | 108 | 48 | 15 |
50 | 31 | 26 | 15 | 7 |
��pH�����ܼ���O3�ֽ⣬������O3�ֽ�������õ���___________.��
����30��C��pH=4.0�����£�O3�ķֽ�����Ϊ__________ mol/(L��min)��
�۾ݱ��еĵݱ���ɣ��Ʋ�O3�����������·ֽ��������������˳��Ϊ______.������ĸ���ţ�
a. 40��C��pH=3.0 b. 10��C��pH=4.0 c. 30��C��pH=7.0
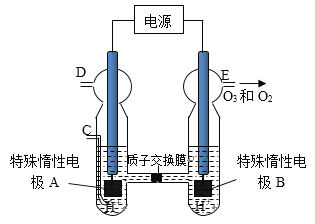
��3��O3 ���ɳ�����������ԭ����ͼ�����ϡ�����Ƶá�
��ͼ������Ϊ_________(�A����B��)����缫��ӦʽΪ_________________.
����C��ͨ��O 2 ����A���ĵ缫��ӦʽΪ_____________________.
����C����ͨ��O 2 ��D��E���ֱ��ռ���xL����yL����(��״��)����E���ռ���������O 3 ��ռ���������Ϊ__________.(����O 3 �ķֽ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����CO����ȼ�ϼ״���һ���¶Ⱥ��ݻ������·�����Ӧ��CO(g)+2H2(g)![]() CH3OH(g)��ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
CH3OH(g)��ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��

��ش��������⣺
��1���ڡ�ͼ1���У�����_______(�a����b��)��ʾʹ���˴�����û��ʹ�ô���ʱ���ڸ��¶Ⱥ�ѹǿ�����·�ӦCO(g)+2H2(g)![]() CH3OH(g)����H=_________��
CH3OH(g)����H=_________��
��2���ӷ�Ӧ��ʼ������ƽ�⣬v(CO)=________���ﵽƽ��ʱ�����¶���CO(g)+2H2(g) ![]() CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ______________���ﵽƽ��������������������䣬���������ѹ ��Ϊ0.5L����ƽ��___________�ƶ� (�������������)��
CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ______________���ﵽƽ��������������������䣬���������ѹ ��Ϊ0.5L����ƽ��___________�ƶ� (�������������)��
��3����֪CH3OH(g)��3/2O2(g)��CO2(g)��2H2O(g)����H����193kJ/mol����֪H2O(l)= H2O(g)����H����44 kJ/mol����д��32g��CH3OH(g)��ȫȼ������Һ̬ˮ���Ȼ�ѧ����ʽ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.��ͼ��ʾ���ס�����װ�õ缫���϶���������̼������ش��������⣺
(1)����װ���о�ΪCuSO4��Һ����Ӧһ��ʱ���
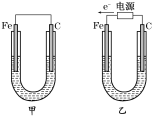
���к�ɫ���������ķֱ��Ǽס���װ���е�________��
A.���е�Fe�������е�Fe�� B.���е�C�������е�Fe��
C. ���е�C �������е�Fe�� D.���е�C�������е�C��
����װ���������ĵ缫��Ӧʽ�ǣ�____________________________________________��
(2)����װ���о�Ϊ����NaCl��Һ��
��д����װ�����ܷ�Ӧ�����ӷ���ʽ��_________________________________________��
�ڽ�ʪ��ĵ���KI��ֽ������װ��̼��������������ֽ������������ԭ��___________��
��.��ͼΪ��ɫ��Դ������ȼ�ϵ�ء��Ĺ���ԭ��ʾ��ͼ��
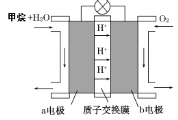
�����ĵ缫��ӦΪ______________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ҹ涨������ʳ�����Ậ����Ϊ3.5��5.0 g/100 mL�����Ậ����100 mLʳ����CH3COOH����������ij��ѧ��ȤС��Ϊ�ⶨij����ʳ�����Ậ����������ʵ�飮ʵ���֪10.0mL��ʳ����Ʒ��7.5 g���ʵ���������Ϊ4%������������Һǡ����ȫ��Ӧ�����������ʳ����Ʒ�е����Ậ������˵���Ƿ���Ϲ��ұ��������������ʳ����Ʒ���������ʲ����������Ʒ�����Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��ͬ�¶���ˮ��Һ��c(H��)��c(OH��)�Ĺ�ϵ�������ж���ȷ����( )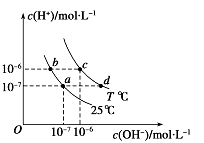
A.ֻ�������µķ�ʽ������a����d��
B.T��25
C.b���c��pH��Ϊ6����Һ������
D.������������������c (H��) ��c (OH��)��Kw
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС���ͬѧΪ̽��ԭ���ԭ���������ͼ��ʾװ�ã���п��ͭͨ����������������ϡ�����С�
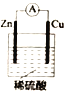
��1��пƬ�ϵĵ缫��ӦʽΪ__________________��
��2��ͭƬ�ϵ�������__________________��
��3������Ӧ��������0.2 mol���ӷ���ת�ƣ������ɵ������ڱ�״���µ����Ϊ______________��
��4����С��ͬѧ��ϡ����ֱ������Լ����������Ի�ƫת����_________������ţ���
A����ˮ�Ҵ� B��������Һ C��CuSO4��Һ D����
��5��ʵ���ͬѧ�Ǿ���������ۣ���Ϊ����ijЩҪ��Ļ�ѧ��Ӧ������ͨ��ԭ�����ʵ�֡����з�Ӧ������Ƴ�ԭ��ص���________������ĸ���ţ���
A�� NaOH+HCl= NaCl+H2O B�� 2H2+O2=2H2O
C�� Fe+2FeCl3=3FeCl2 D�� 2H2O=2H2��+2O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ�ý���ʵ�飬��ʼʱ��a��b����Һ����ƽ���ܷ�ã�����һ��ʱ�䡣����˵������ȷ���� (����) 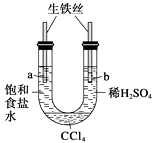
A.a�ܷ���������ʴ��b�ܷ������ⸯʴ
B.һ��ʱ���a��Һ�����b��Һ��
C.a����Һ��pH����b����Һ��pH��С
D.a��b����������ͬ�ĵ缫��Ӧʽ��Fe��2e���� Fe2��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com