
| A. | 测定中和热时,所用稀NaOH溶液和HCl的物质的量恰好相等,以减小实验误差 | |
| B. | NaHSO4固体受热变为熔融状态(未发生化学反应),需要克服的作用力有:离子键和共价键 | |
| C. | 在Fe(OH)3胶体中通电,一段时间后,阴极附近颜色加深 | |
| D. | 用蒸馏的方法分离淀粉溶液与Cu(OH)2悬浊液的混合物 |
分析 A.测定中和热时,应使盐酸完全反应,减小实验误差;
B.硫酸氢钠固体熔化时只破坏离子键,不破坏共价键;
C.氢氧化铁胶粒带正电荷;
D.浊液和胶体用过滤来分离;
解答 解:A.测定中和热时,应加入稍过量的氢氧化钠,使盐酸完全反应,减小实验误差,故A错误;
B.硫酸氢钠固体熔化时电离出钠离子和硫酸氢根离子,所以只破坏离子键不破坏共价键,故B错误;
C.氢氧化铁胶粒带正电荷,通电时向阴极移动,一段时间后,阴极附近颜色加深,故C正确;
D.用过滤的方法分离淀粉溶液与Cu(OH)2悬浊液的混合物,故D错误;
故选C.
点评 本题考查较为综合,涉及物质的性质、分离、中和热测定等知识,侧重于学生的分析能力能力和实验能力的考查,难度不大.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂化主要得到乙烯 | |
| B. | 石油分馏是化学变化,可得到汽油、煤油 | |
| C. | 煤的干馏是化学变化,可以得到出炉煤气、煤焦油和焦炭 | |
| D. | 煤的气化是物理变化,是高效、清洁地利用煤的途径 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
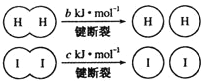
| A. | 向密闭容器中加入1 mol H2(g)和2mol I2(g),充分反应后放出的热量有可能等于a kJ | |
| B. | 反应物的总能量低于生成物的总能量 | |
| C. | 断开2 mol H-I键所需能量约为(c+b+a)kJ | |
| D. | 断开1 mol I-I键的同时形成2mol H-I键,说明反应已达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
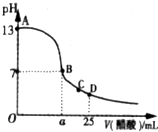 在25mL的氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,滴定曲线如图所示.
在25mL的氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,滴定曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
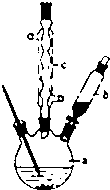 苯乙酸铜是合成优良催化剂、传感材料-纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料-纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线: (苯乙腈)
(苯乙腈)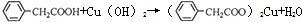
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
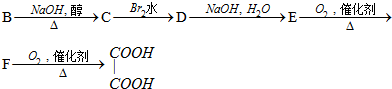

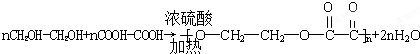 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
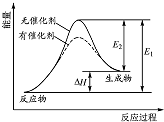
| A. | 该反应的反应物总能量高于生成物总能量 | |
| B. | 使用催化剂可以增大该反应的反应热 | |
| C. | 该化学反应的反应热为E1,且反应放热 | |
| D. | 化学反应在物质变化的同时,必然伴随能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com