
【题目】基于CaSO4为载氧体的天然气燃烧是一种新型绿色的燃烧方式,CaSO4作为氧和热量的有效载体,能够高效低能耗地实现CO2的分离和捕获其原理如下图所示:
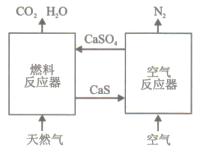
(1)已知在燃料反应器中发生如下反应:
i.4CaSO4(s)+CH4(g)=4CaO(s)+CO2(g)+4SO2(g)+2H2O(g) ΔH1=akJ/mol
ii.CaSO4(s)+CH4(g)=CaS(s)+CO2(g)+2H2O(g) ΔH2=bkJ/mol
ⅲ. CaS(s)+3CaSO4(s)= 4CaO(s)+4SO2(g) ΔH3=ckJ/mol
①燃料反应器中主反应为_________(填“i”“ii”或“ⅲ”)。
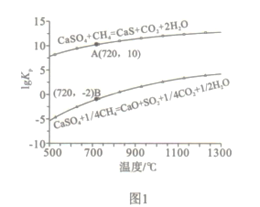
②反应i和ii的平衡常数Kp与温度的关系如图1,则a_______0(填“ >”“ =“或“<” );720℃时反应ⅲ的平衡常数Kp=________。
③下列措施可提高反应ii中甲烷平衡转化率的是_______。
A.增加CaSO4固体的投入量 B.将水蒸气冷凝
C.降温 D.增大甲烷流量
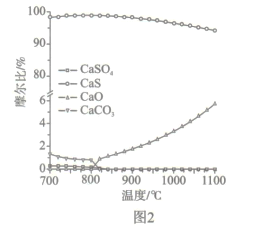
(2)如图2所示,该燃料反应器最佳温度范围为850℃ -900℃之间,从化学反应原理的角度说明原因:_______。
(3)空气反应器中发生的反应为
CaS(s) +2O2(g)=CaSO4(s) ΔH4=dkJ/mol
①根据热化学原理推测该反应为__________反应。
②在天然气燃烧过程中,可循环利用的物质为________。
(4)该原理总反应的热化学方程式为____________
【答案】 ii > 1.0×10-18 B 温度过低,反应速率较慢 ;温度较高,副反应增多 放热 CaS、CaSO4 CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=(b+d)kJ/mol或ΔH=(a-c+d)kJ/mol
【解析】(1)①由图示可得,天然气和CaSO4进入燃料反应器,反应生成CaS、CO2和H2O,故燃料反应器中主反应为ii。②由图1可看出,温度越高lgKp越大,即升温Kp增大,故反应i和反应ii都是吸热反应,则a和b都大于0。设三个反应的平衡常数Kp分别为:Kpi、Kpii、Kpⅲ,根据盖斯定律,i-ii得ⅲ,所以Kpⅲ=![]() ;由图并结合热化学方程式可得720℃时反应i的lgKp为:-2×4=-8,反应ii的lgKp为10,所以Kpi=10-8,Kpii=1010,故Kpⅲ=
;由图并结合热化学方程式可得720℃时反应i的lgKp为:-2×4=-8,反应ii的lgKp为10,所以Kpi=10-8,Kpii=1010,故Kpⅲ=![]() =
=![]() =1.0×10-18。③A项,增加固体物质的投入量,不改变化学平衡,所以增加CaSO4固体的投入量不能提高反应ii中甲烷平衡转化率,故A错误;B项,将生成物分离出去能使化学平衡正向移动,所以将水蒸气冷凝能提高反应ii中甲烷平衡转化率,故B正确;C项,通过②的分析,该反应为吸热反应,降温能降低反应ii中甲烷平衡转化率,故C错误;D项,增大甲烷流量,增大了甲烷的浓度,平衡正向移动,但根据勒沙特列原理,甲烷平衡转化率会降低,故D错误。
=1.0×10-18。③A项,增加固体物质的投入量,不改变化学平衡,所以增加CaSO4固体的投入量不能提高反应ii中甲烷平衡转化率,故A错误;B项,将生成物分离出去能使化学平衡正向移动,所以将水蒸气冷凝能提高反应ii中甲烷平衡转化率,故B正确;C项,通过②的分析,该反应为吸热反应,降温能降低反应ii中甲烷平衡转化率,故C错误;D项,增大甲烷流量,增大了甲烷的浓度,平衡正向移动,但根据勒沙特列原理,甲烷平衡转化率会降低,故D错误。
(2)从反应速率角度考虑,温度过低,反应速率较慢,应在较高温度下反应,但由图2可得,温度越高,副反应增多,所以该燃料反应器最佳温度范围为850℃~900℃之间。
(3)①由方程式可看出该反应S<0,因为自发反应H-TS<0,所以H<0,故该反应为放热反应。②空气反应器中CaS和O2反应生成CaSO4,燃料反应器中,天然气和CaSO4反应生成CaS、CO2和H2O,所以在天然气燃烧过程中可循环利用的物质为:CaS和CaSO4。
(4)将反应CaS(s) +2O2(g)=CaSO4(s) ΔH4=dkJ/mol标号为iiii,分析空气反应器中发生的反应和燃料反应器中发生的反应,根据盖斯定律,ii+iiii或i-iii+iiii得该原理总反应的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=(b+d)kJ/mol或ΔH=(a-c+d)kJ/mol。


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列有关说法不正确的是
A. 由1mol CH3OCOONa和少量CH3COOH形成的中性溶液中,CH3COO-数目是NA
B. 1.68gFe与足量高温水蒸气反应,转移电子的数目为0.09NA
C. 氢原子数为0.4NA的CH3OH 分子中含有的电子数为1.8NA
D. 常温下,2L 0.1molL-1FeCl3溶液与1L0.2molL-1FeCl3溶液所含Fe3+数目不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电池叙述正确的是( )
A.水果电池是高效环保的家用电池
B.锌锰干电池是一种常用的二次电池
C.锌锰干电池碳棒是负极,锌片是正极
D.锌锰干电池工作一段时间后锌外壳逐渐变薄
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铝分别和O2、O3发生反应生成Al2O3 , 反应过程和能量关系如下图所示(图中的ΔH表示生成1 mol产物的数据)。下列有关说法中不正确的是( )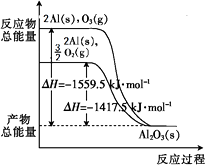
A.Al(s)与O3(g)反应的热化学方程式为2Al(s)+O3(g)=Al2O3(s) ΔH =-1559.5 kJ·mol-1
B.等质量的O2比O3的能量低
C.1 mol O2完全转化为O3 , 需吸收142 kJ的热量
D.给3O2(g) ![]() 2O3(g)的平衡体系加热,有利于O3的生成
2O3(g)的平衡体系加热,有利于O3的生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应aA(g)+bB(s) ![]() cC(g)+dD(g),在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是( )
cC(g)+dD(g),在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是( ) 
A.温度降低,化学平衡向逆反应方向移动
B.使用催化剂,C的物质的量分数增加
C.化学方程式系数a<c+d
D.平衡时再加入A,平衡向右移动,A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2(g)+I2(g) ![]() 2HI(g)△H<0。相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。下列说法错误的是( )
2HI(g)△H<0。相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。下列说法错误的是( )
A.反应放出的热量一定相同
B.此时体系的压强一定相同
C.反应物的转化率可能相同
D.此时HI的浓度一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X,Y,Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X和Y组成原电池时,Y为电池的负极.X,Y,Z三种金属的活动性顺序为( )
A.X>Y>Z
B.X>Z>Y
C.Y>X>Z
D.Y>Z>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一固定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2 ![]() 2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量的NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2 , 气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。请回答下列问题(计算结果保留一位小数):
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量的NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2 , 气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。请回答下列问题(计算结果保留一位小数):
(1)判断该反应达到平衡状态的标志是。(填字母)
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.容器中气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.向装置中再充入SO3
(3)求该反应达到平衡时SO2的转化率为(用百分数表示)。
(4)若将平衡混合气体的5%通入过量的Ba(OH)2溶液,生成沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,按化合物、单质、混合物顺序排列的是( )
A.烧碱、液态氧、碘酒B.生石灰、白磷、熟石灰
C.干冰、水银、氯化氢D.空气、氮气、胆矾
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com