
����Ŀ�����������ܣ�Co2O3����Ҫ�������ϡ����ϡ����Բ��ϡ��������������ȡ��Ժ��ܷ��ϣ���Ҫ�ɷ�ΪCo2O3����������MnO2��NiO��Fe3O4��Ϊԭ���Ʊ�Co2O3����������ͼ��ʾ��

��֪��
��.���������Ľ���Һ�к�����������H+��Co2+��Fe3+��Ni2+�ȡ�
��.����������������������ʽ����ʱ��Һ��pH���±���
������ | Fe(OH)3 | Co(OH)2 | Ni(OH)2 |
��ȫ����ʱ��pH | 3.7 | 9.0 | 9.2 |
�ش��������⣺
(1)����������ܷ��ϵ��¶Ȳ��˹��ߣ�ԭ����_____________��
(2) �������ʱ��������Ҫ��Ӧ��___________________��д���ӷ���ʽ����
(3)ij��ȡ���Խ������ӵ���ȡ������ҺpH�Ĺ�ϵ��ͼ��ʾ��
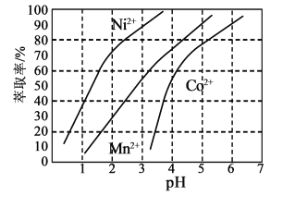
ʹ�ø���ȡ��ʱӦ���Ƶ�pHԼΪ____________��������_____________��
(4)д����������ʱ�����Ļ�ѧ��Ӧ����ʽ___________��
(5)����1�õ��ĸ���Ʒ��__________�������ƣ���
��֪�����ʵ���Һ���ȵ�100��ʱ����ʣ������ʵ��ܽ�ȼ��±���
ʪ�� | 0�� | 10�� | 20�� | 30�� | 40�� | 50�� | 60�� |
�ܽ�� | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 88.0 |
����1��________������ĸ����
a�������ᾧ b�����½ᾧ c����ѹ�����ᾧ
(6)�л�����ȡ��Ni2+����ʱ�������Ʊ������أ��õ�س��ʱ���ܷ�ӦΪNi(OH)2+M=NiOOH+MH����ŵ�ʱ�����ĵ缫��ӦʽΪ_________________��
���𰸡��¶ȹ���H2O2���ֽ� Co2O3+H2O2+4H+=2Co2++3H2O+O2�� 2.5��3.3���� ��ȡ���ڸ�pHʱ��Ni2+��Co2+��ȡ�ʲ����ܷ���Ni2+��Co2+�������� 2Co2(OH)2CO3+O2![]() Co2O3+2H2O+2CO2 ����� c MH+OH- - e- =M+H2O
Co2O3+2H2O+2CO2 ����� c MH+OH- - e- =M+H2O
��������
���ܷ���(��Ҫ�ɷ�ΪCo2O3����������MnO2��NiO��Fe3O4)�м��������H2O2�����MnO2���ܣ��������ʶ��ܽ⣬�Ӻ��������Co2O3��H2O2��ԭΪCo2+��Fe3O4�ܽ⣬ͬʱ���ɵ�Fe2+������ΪFe3+����pH��3.7��Fe3+ת��ΪFe(OH)3������������ȡ����Ni2+�����л��࣬Co2+����ˮ�ࣻ����NH4HCO3�Ͱ�ˮ��Co2+ת��ΪCo2(OH)2CO3��������Һ��Ӧ����(NH4)2SO4����������ʱ��Co2(OH)2CO3��Co2+��+2���ߵ�+3�����ǼķֽⷴӦ�����Ƿֽ��������O2��Ӧ������Co2O3��H2O��CO2��
(1)˫��ˮ���ȶ��Բ����������ܷ��ϵ��¶Ȳ��˹��ߣ�ԭ�����¶ȹ���H2O2���ֽ⡣��Ϊ���¶ȹ���H2O2���ֽ⣻
(2) �������ʱ��Co2O3��H2O2��ԭΪCo2+����������Ҫ��Ӧ��Co2O3+H2O2+4H+=2Co2++3H2O+O2������Ϊ��Co2O3+H2O2+4H+=2Co2++3H2O+O2����
(3)ʹ�ø���ȡ����ȡNi2+����������ȡ�ʿ��ǣ���ȡ��Խ��Խ�ã���ͬʱ���迼�ǵ���Co2+�����ܲ�����ȡ���������ۺϿ��ǣ�Ӧ���Ƶ�pHԼΪ2.5��3.3���ɣ���������ȡ���ڸ�pHʱ��Ni2+��Co2+��ȡ�ʲ����ܷ���Ni2+��Co2+�������ӡ���Ϊ��2.5��3.3���ɣ���ȡ���ڸ�pHʱ��Ni2+��Co2+��ȡ�ʲ����ܷ���Ni2+��Co2+�������ӣ�
(4)��������ʱ��Co2(OH)2CO3�ķֽ���ﱻO2��������Co2O3�ȣ���ѧ��Ӧ����ʽ2Co2(OH)2CO3+O2![]() Co2O3+2H2O+2CO2����Ϊ��2Co2(OH)2CO3+O2
Co2O3+2H2O+2CO2������2Co2(OH)2CO3+O2![]() Co2O3+2H2O+2CO2��
Co2O3+2H2O+2CO2��
(5)�ɷ���֪������1�õ��ĸ���Ʒ������李���Ϊ������泥����ܽ�ȱ���������淋��ܽ�����¶��������������仯������������������ֽ⣬���Բ���1�Ǽ�ѹ�����ᾧ����ѡc����Ϊ��c��
(6)�ŵ�ʱ����ΪMHʧ��������M�ȣ��缫��ӦʽΪMH+OH- - e- =M+HO����Ϊ��MH+OH- - e- =M+H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NiS �������մɺ��´ɵ���ɫ����NiS ����ˮ����ʱ�ܱ�����������Ni(OH)S����H2Sͨ��ϡ�����ữ��NiSO4��Һ�У��������ˣ��Ƶ�NiS ������װ����ͼ��ʾ:

���ж�ʵ���������ȷ����
A. ��װ��A�еμ�����ˮǰͨ��N2����Ϊ�˽�H2S����C װ������NiSO4��Һ��Ӧ
B. װ��B ��ʢ��Ũ����
C. װ��D �е�ϴ��ҺӦ����й�������ˮ
D. ��Ӧ���������ͨ��N2 �ɽ�Cװ���в����ij���ѹ����˳���©����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֤����������������������ʵ���������ձ��ھ�Ϊ�����ữ��3%NaCl��Һ����
�� | �� | �� |
|
|
|
��Fe����������ɫ���� | �Թ��������Ա仯 | �Թ���������ɫ���� |
����˵������ȷ����
A. �Ա��ڢۣ������ж�Zn������Fe
B. �Ա��٢ڣ�K3[Fe(CN)6]���ܽ�Fe����
C. ��֤Zn����Feʱ���������ķ���
D. ��Zn����Cu�������ķ������ж�Fe��Cu����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���Mֻ��C��H��O����Ԫ�ء�ȡ13.6g M������������ȼ�գ�����35.2g CO2��7.2g H2O������ͬ�����£�M������������������ܶ�Ϊ68��
��1��ͨ������ȷ��M�ķ���ʽ����Ҫ��д��������̣�____________��
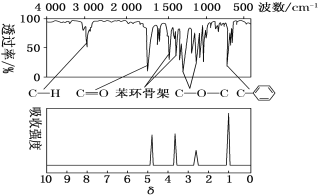
��2�����ⶨ��M�ĺ�����ͺ˴Ź������ֱ�����ͼ��ʾ����M�Ľṹ��ʽΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ��
��![]() ��������Ҫ���������壬��
��������Ҫ���������壬��![]() ��
��![]() Ϊԭ���������ֵ�Ļ�ѧ��Ʒ��������������ЧӦ���о����ش��������⣺
Ϊԭ���������ֵ�Ļ�ѧ��Ʒ��������������ЧӦ���о����ش��������⣺
(1)��ҵ��![]() ��������Ŀǰ���ģ��ȡ�ϳ�����CO��H2�������Ϊ�ϳ���������Ҫ��������ԭ��Ϊ��
��������Ŀǰ���ģ��ȡ�ϳ�����CO��H2�������Ϊ�ϳ���������Ҫ��������ԭ��Ϊ��
��Ӧ��![]() ��
��![]()
��Ӧ��![]() ��
��![]()
![]() ��
��![]() ��Ӧ����
��Ӧ����![]() ��
��![]() ���Ȼ�ѧ����ʽ��___________________��
���Ȼ�ѧ����ʽ��___________________��
(2)��1 mol ![]() ��1 mol
��1 mol ![]() ������º�ѹ���ܱ������У��¶�298K��ѹǿ100kPa����������Ӧ�����Ƿ�Ӧ��ķ������÷�Ӧ�У�����Ӧ����
������º�ѹ���ܱ������У��¶�298K��ѹǿ100kPa����������Ӧ�����Ƿ�Ӧ��ķ������÷�Ӧ�У�����Ӧ����![]() ��pΪ��ѹ����ѹ=��ѹ�����ʵ���������������������
��pΪ��ѹ����ѹ=��ѹ�����ʵ���������������������![]() ����
����![]() �ֽ�20%ʱ��
�ֽ�20%ʱ��![]() __________kPas-1��
__________kPas-1��
(3)��![]() ��
��![]() ��һ�������·�Ӧ���Ƶúϳ�������1 L�ܱ�������ͨ��
��һ�������·�Ӧ���Ƶúϳ�������1 L�ܱ�������ͨ��![]() ��
��![]() ��ʹ�����ʵ���Ũ�Ⱦ�Ϊ
��ʹ�����ʵ���Ũ�Ⱦ�Ϊ![]() ����һ�������·�����Ӧ��
����һ�������·�����Ӧ�������CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��
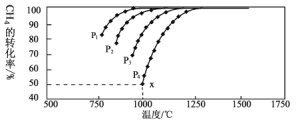
��ѹǿ![]() ��
��![]() ��
��![]() ��
��![]() ��С����Ĺ�ϵΪ_________��
��С����Ĺ�ϵΪ_________��
�ڶ������෴Ӧ����ij��֣�B����ƽ��ѹǿp(B)�������ʵ���Ũ��c(B)Ҳ�ɱ�ʾƽ�ⳣ��������![]() �������
�������![]() ����x���ƽ�ⳣ��
����x���ƽ�ⳣ��![]() ________________����ƽ���ѹ����ƽ��Ũ�ȼ��㣩��
________________����ƽ���ѹ����ƽ��Ũ�ȼ��㣩��
�����д�ʩ����ʹƽ�������ƶ�����___________������ĸ����
a�������¶�
b������ѹǿ
c�������¶ȡ�ѹǿ���䣬����He
d�����¡����ݣ��ٳ���1 mol ![]() ��1 mol
��1 mol ![]()
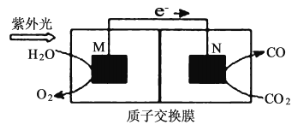
(4)��ѧ�һ��о�������ת����������ķ���������ͼ��ʾװ�ÿ��Խ�![]() ת��Ϊ����ȼ��CO���������ҺΪϡ���ᣩ����װ�ù���ʱ��MΪ_________�����������������������ͨ��2 mol���Ӻٶ��������M���������Һ��pH__________�����������С�����䡱����N���������Һ�仯������
ת��Ϊ����ȼ��CO���������ҺΪϡ���ᣩ����װ�ù���ʱ��MΪ_________�����������������������ͨ��2 mol���Ӻٶ��������M���������Һ��pH__________�����������С�����䡱����N���������Һ�仯������![]() __________g��
__________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ�������ֵ������������ȷ���ǣ� ��
A. 60g�����д��ڵĹ��ۼ�����Ϊ10NA
B. 1L 0.1mol��L��1��NaHCO3��Һ��HCO3����CO32��������֮��Ϊ0.1NA
C. ���ڿ�����ȼ�տ����ɶ��������23g�Ƴ��ȼ��ʱת�Ƶ�����Ϊ1NA
D. 235g�˻�U![]() �����ѱ䷴Ӧ��
�����ѱ䷴Ӧ��![]() +
+![]() n
n![]()
![]() +
+![]() +10
+10![]() n��������������(
n��������������(![]() n)��Ϊ10NA
n)��Ϊ10NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ת������Դ���úͻ�����������Ҫ�о����⡣��H2S�Ϳ����Ļ������ͨ��FeCl3��FeCl2��CuCl2�Ļ����Һ�л���S����ת����ͼ��ʾ��CuS������ˮ��������˵���У�����ȷ���ǣ� ��

A.���̢��У�����CuS�ķ�ӦΪH2S+Cu2+=CuS��+2H+
B.���̢��У�Fe3+��������
C.ת��ͼ�л��ϼ۲����Ԫ��ֻ��ͭ����
D.����S���ܷ�ӦΪ2H2S+O2=2H2O+2S��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���������ȷ����
A. ![]()
B. ![]()
C. 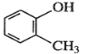 ������
������
D. (CH3)2C��CH(CH2)2CH3 2-��-2-��ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ᣨH2N2O2����һ�ֶ�Ԫ�ᣬ�����£���0.01mol��L-1��NaOH��Һ�ζ�10mL0.01mol��L-1��H2N2O2��Һ�������ҺpH��NaOH��Һ����Ĺ�ϵ��ͼ�������£����и�������Ӧ��Һ�������ʵ���Ũ�ȹ�ϵ��ȷ���ǣ� ��

A.a�㣺c(N2O22-)��c(HN2O2-)-c(Na��)=9.9��10-7mol��L-1
B.b�㣺c(Na��)��c(N2O22-)��c(HN2O2-)��c(H2N2O2)
C.c�㣺c(Na��)��c(HN2O2-)��c(N2O22-)��c(H2N2O2)
D.d�㣺2c(H2N2O2)��c(HN2O2-)��c(H+)=c(OH-)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com