
【题目】如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓![]() 溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验中,不考虑两球的浮力变化)( )
溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验中,不考虑两球的浮力变化)( )
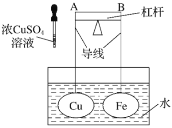
A.杠杆为导体或绝缘体时,均为A端高B端低
B.杠杆为导体或绝缘体时,均为A端低B端高
C.当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高
D.当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】过碳酸钠俗称固体双氧水,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,它的制备原理和路线如下:
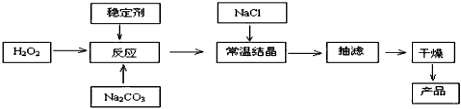
已知:2Na2CO3 + 3H2O2 =2Na2CO3·3H2O2 △H<0
请回答下列问题:
(1)下列物质可使过碳酸钠较快失效的是_________________。
a.MnO2 b.H2S c.稀硫酸 d.NaHCO3
(2)加入NaCl的作用是_________________。
(3)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与Fe3+生成稳定的配合物,Fe3+对反应的不良影响是_________________。
(4)反应的最佳温度控制在15℃~20℃,温度偏高时造成产率低可能是_________________。
(5)以上流程中遗漏了一步,造成所得产品纯度偏低,该步操作的名称是_________________。进行该操作的方法是:_________________。
(6)为测定产品的纯度。
准确称取ag产品配成250mL溶液,移取25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释成100mL,作被测试样;用高锰酸钾标准溶液滴定被测试样,MnO4-的还原产物是Mn2+。用cmol/L KMnO4标准溶液VmL滴定待测液,滴定到达终点的现象是________________。
重复滴定三次,平均消耗cmol/L KMnO4标准溶液VmL,则产品中过碳酸钠的质量分数为______________。配制cmol/L KMnO4标准溶液时,移液时有少量液体溅出,则产品的纯度将_________(变大、变小或不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粉煤灰中的氮可通过如图所示方法处理生成对环境无影响的氮气,下列说法正确的是
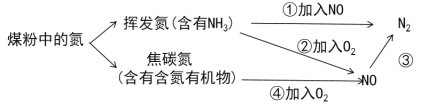
A.反应③中加入的物质可以是空气或氨气
B.反应①中,每生成22.4L(标况下)N2,转移电子2.4mol
C.用湿润的蓝色石蕊试纸可判断挥发氮中含有NH3
D.焦碳氮在空气中充分燃烧产生的尾气可直接排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种重要的化工原料,依据题给信息,回答下列问题:
Ⅰ.碳酸钠可利用CO2采用氨碱法生产
(1)碳酸钠可作为碱使用的原因是_____________(用离子方程式表示)。
(2)已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) ΔH1=127.4 kJ/mol
②NaOH(s)+CO2(g)=NaHCO3(s) ΔH2=131.5kJ/mol
反应2NaHCO3(s)=Na2CO3(s)+ H2O(g) +CO2(g)的ΔH=___________ kJ/mol。
Ⅱ.在体积为2 L的密闭容器中,充入1mol/LCO2 和1mol/L H2,进行如下化学反应:
CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 | |||
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为____________反应(选填吸热、放热)。
(2)能判断该反应是否达到化学平衡状态的依据是_______________。
a.容器中压强不变 b.混合气体中 c(CO)不变
c. υ正(H2)=υ逆(H2O) d. c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为____________℃。
(4)某温度下经2min反应达到平衡后c(CO)=0.8mol/L,此温度下的平衡常数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Ⅰ:CaSO4(s)+ CO(g) ![]() CaO(s)+SO2(g)+CO2(g) ΔH=+218.4 kJ·mol-1反应Ⅱ:CaSO4(s)+4CO(g)
CaO(s)+SO2(g)+CO2(g) ΔH=+218.4 kJ·mol-1反应Ⅱ:CaSO4(s)+4CO(g) ![]() CaS(s)+4CO2(g) ΔH=-175.6 kJ·mol-1假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是
CaS(s)+4CO2(g) ΔH=-175.6 kJ·mol-1假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是
A.  B.
B. 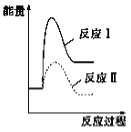 C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在T ℃时,铬酸银(Ag2CrO4)在水溶液中的沉淀溶解平衡曲线如图所示。下列说法中不正确的是
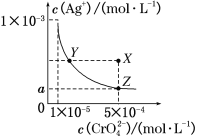
A. T ℃时,在Y点和Z点,Ag2CrO4的Ksp相等
B. 向饱和Ag2CrO4溶液中加入固体K2CrO4不能使溶液由Y点变为X点
C. 图中a=![]() ×10-4
×10-4
D. T ℃时,Ag2CrO4的Ksp为1×10-8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型锌碘液流电池具有能量密度高、循环寿命长等优势,其工作原理如图所示。下列说法错误的是

A. 放电时电流从石墨电极流向锌电极
B. 充电时阳极反应式为:3I--2e-=I3-
C. 若将阳离子交换膜换成阴离子交换膜,放电时正负极也随之改变
D. 放电时左侧电解质储罐中的离子总浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | ④ | ||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
回答下列问题:
(1)元素①的名称是____,元素⑧的符号是____。
(2)在这些元素中,___(用元素符号或化学式填写,下同)是最活泼的非金属元素,____是最不活泼的元素。
(3)这些元素的最高价氧化物对应的水化物中,____酸性最强,____碱性最强,具有两性的氢氧化物是____。
(4)比较⑤与⑥的化学性质,____更活泼,试用实验证明此结论(简述操作、现象和结论):________________________。
(5)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯的叠氮酸(HN3)是一种弱酸,常温下向25mL 0.1 mol/L NaOH溶液中加入0.2 mol/L HN3溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如下图。下列说法正确的是( )
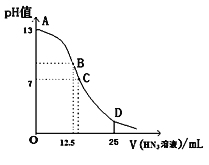
A. 该滴定过程中应用甲基橙作指示剂
B. 若B点pH=8,则c(HN3)=(10-6~10-8 )mol/L
C. 点D对应溶液中存在关系:c(HN3)>c(Na+)>c(N3-)
D. 沿曲线A→B→C的过程中,由水电离产生的c(OH-)逐渐减少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com