
(1)一定条件下的密闭容器中,反应3H2(g)+3CO(g) CH3OCH3(二甲醚)(g)+CO2(g) ΔH<0达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。 [
CH3OCH3(二甲醚)(g)+CO2(g) ΔH<0达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。 [
a.升高温度 b.加入催化剂 c.减小CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(2)已知反应②2CH3OH(g) CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
①比较此时正、逆反应速率的大小:v(正) v(逆)(填“>”“<”或“=”)。
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH)= ;该时间内反应速率v(CH3OH)= 。
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
Ⅰ:元素X、Y、Z、E、M、N均为短周期主族元素,且原子序数依次增大。已知Y元素原子最外层电子数与核外电子总数之比为3∶4,M元素与 Y元素能形成化合物MY2和化合物MY3,化合物MY2中两种元素质量分数相同;N-、Z+、X+的半径逐渐减小;化合物XN在常温下为气体,E、Z、N的最高价氧化物的水化物两两能反应,回答下列问题:
(1)写出Z最高价氧化物的水化物的电子式 ____________________。
(2)两个体积相等的恒容容器,甲容器通入1 mol MY2和1 mol Y2单质,乙容器通入1 mol MY3和0.5 mol Y2单质,发生反应:2 MY2 (g) + Y2(g)  2 MY3(g) △H<0,甲、乙起始反应温度相同,两容器均和外界无热量交换,平衡时,甲中MY2的转化率为a,乙中MY3的分解率为b,则
2 MY3(g) △H<0,甲、乙起始反应温度相同,两容器均和外界无热量交换,平衡时,甲中MY2的转化率为a,乙中MY3的分解率为b,则
①a、b的关系为a+b 1(填“﹤”、“﹥”或“=”) 。
②该条件下容器甲反应达平衡状态的依据是(填序号) 。
A.v正(Y2)=2v逆(MY3) B.混合气体的密度不变
C.c(MY2)=c(MY3) D.混合气体的总物质的量不变
E、容器内温度不变 F、MY2和Y2的质量比不变
(3)2.7克单质E与100ml 2mol/L Z的最高价氧化物的水化物充分反应,向反应后的溶液中滴入2 mol/L XN的溶液V ml,当溶液中产生3.9克沉淀时,求此时V的值 (写出计算过程)
Ⅱ:(4)已知在常温常压下:

(5)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池负极的电极反应式为_ ___
②若以该电池为电源,用石墨做电极电解200mL含有如下离子的溶液.

电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上发生的电极反应 。
查看答案和解析>>
科目:高中化学 来源: 题型:
书写下列物质在水溶液中的电离方程式:
CH3COOH:__________________________________
Ca(OH)2:___________________________________
NH3.H2O:________________________ ________________
NH4HSO4:________________________________________
H2CO3:_______________________________________________
NaHCO3:_______________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,向容积固定的密闭容器里充入a mol N2O4发生如下反应:N2O4 (气) 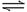 2NO2 (气),达到平衡后,再向该容器内充入a mol N2O4,达平衡后与原平衡比较正确的是 ( )
2NO2 (气),达到平衡后,再向该容器内充入a mol N2O4,达平衡后与原平衡比较正确的是 ( )
A.平均相对分子质量减小 B.N2O4的转化率提高
C.压强为原来的2倍 D.颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示。下列判断正确的是( )

A.在0~50 min之间,pH=2和pH=7时R的降解百分率相等
B.溶液酸性越强,R的降解速率越小
C.R的起始浓度越小,降解速率越大
D.在20~25 min之间,pH=10时R的平均降解速率为 0.04 mol·(L·min)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如右图所示,下列说法正确的是
A.a、b、c三点溶液的pH:c<a<b
B.a、b、c三点醋酸的电离程度:a<b<c
C.用湿润的pH试纸测量a处溶液的pH,测量结果偏大
D.a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:c<a<b

查看答案和解析>>
科目:高中化学 来源: 题型:
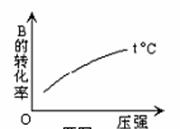
可逆反应 A(气) + nB(气)  2C(气) (正反应吸热)在一定温度下,反应物 B 的转化率与压强有如图所示的关系,那么 n 值一定是( )
2C(气) (正反应吸热)在一定温度下,反应物 B 的转化率与压强有如图所示的关系,那么 n 值一定是( )
A.>1 B.≥ 1 C.1 D. 2
查看答案和解析>>
科目:高中化学 来源: 题型:
氯碱工业是最基本的化学工业之一,离子膜电解法为目前普遍使用的生产方法,其生产流程如下图所示:
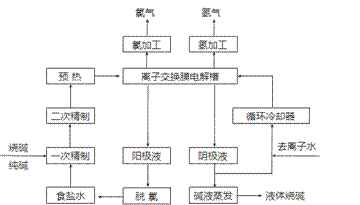
(1)该流程中可以循环的物质是 。
 (2)电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有Ca2+、Mg2+、SO42-等无机杂质,所以在进入电解槽前需要进行两次精制,写出一次精制中发生的离子方程式 ,若食盐水不经过二次精制就直接进入离子膜电解槽会产生什么后果 。
(2)电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有Ca2+、Mg2+、SO42-等无机杂质,所以在进入电解槽前需要进行两次精制,写出一次精制中发生的离子方程式 ,若食盐水不经过二次精制就直接进入离子膜电解槽会产生什么后果 。
(3)右图是工业上电解饱和食盐水的离子交换膜电解槽示意图(阳极用金属钛网制成,阴极由碳钢网制成)。则B处产生的气体是 ,E电极的名称是 。电解总反应的离子方程式为 。
(4)从阳极槽出来的淡盐水中,往往含有少量的溶解氯,需要加入8%~9%的亚硫酸钠溶液将其彻底除去,该反应的化学方程式为 。
(5)已知在电解槽中,每小时通过1安培的直流电可以产生1.492g的烧碱,某工厂用300个电解槽串联生产8小时,制得32%的烧碱溶液(密度为1.342吨/m3)113m3,电解槽的电流强度1.45 ×104A,该电解槽的电解效率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com