
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | Y原子M电子层上有2对成对电子 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的+1价阳离子的核外有3层电子且各层均处于全满状态 |
分析 X、Y、Z、W是元素周期表前四周期中的四种常见元素,X的基态原子核外3个能级上有电子,且每个能级上的电子数相同,X原子核外电子排布式为1s22s22p2,则X为碳元素;Y原子M电子层上有2对成对电子,所以原子核外电子排布式为1s22s22p63s22p4,则Y为硫元素;Z和Y同周期,Z的电负性大于Y,则Z为Cl元素;则W原子核外电子数为2+8+18+1=29,则E为Cu元素,据此解答.
解答 解:X、Y、Z、W是元素周期表前四周期中的四种常见元素,X的基态原子核外3个能级上有电子,且每个能级上的电子数相同,X原子核外电子排布式为1s22s22p2,则X为碳元素;Y原子M电子层上有2对成对电子,所以原子核外电子排布式为1s22s22p63s22p4,则Y为硫元素;Z和Y同周期,Z的电负性大于Y,则Z为Cl元素;则W原子核外电子数为2+8+18+1=29,则E为Cu元素,
(1)Y为硫元素,是第三周期第ⅥA族元素,Y和Z分别为硫元素和Cl元素,非金属性越强其最高价氧化物对应的水化物的酸性越强,所以是非金属氯最高价氧化物对应的水化物,化学式为HClO4,故答案为:第三周期第ⅥA族;HClO4;
(2)CS2是一种常用的溶剂,二硫化碳分子和二氧化碳分子结构相似,根据二氧化碳分子结构知二硫化碳分子中含有存在2个σ键,键的极性和中心原子的得电子能力相关,得电子能力大,极性强,故氢氯键的极性强于氢硫键,键长取决于中心元素的原子半径,半径大,键长长,故氢氯键长于氢硫键;故答案为:2;H-Cl;H-S;
(3)Cu是29号元素,原子核外电子数为29,基态原子核外电子排布式为:1s22s22p63s23p63d104s1,故答案为:1s22s22p63s23p63d104s1.
点评 本题考查了物质的化学性质,正确推断元素是解本题关键,难点是实验设计,根据物质的性质来设计实验即可,难度中等.


科目:高中化学 来源: 题型:解答题
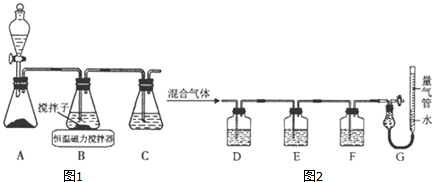
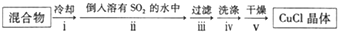
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | b-a=n+m | B. | a-b=n+m | C. | 核电荷数:Y>X | D. | 质子数:Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
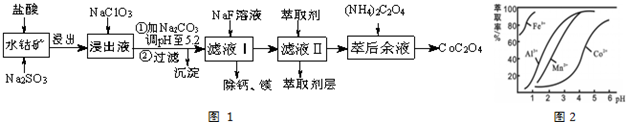
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R在化合物中显+1价 | B. | 最高价氧化物的水化物的碱性:X>R | ||
| C. | 原子半径:W<R<X | D. | R与Z可以形成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝片与稀盐酸的反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | 灼热的炭与CO2的反应 | D. | 硫在氧气中的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
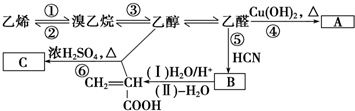
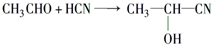 ;加成反应.
;加成反应.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com