
分析 (1)已知0.5mol此有机物的质量为30g,则可以求出其摩尔质量,再根据二氧化碳和水的质量氧元素的质量,然后根据质量守恒求出最简式,根据相对分子质量求出分子式;
(2)根据该有机物的分子式确定其可能的结构简式;
(3)结合有机物性质判断其结构简式及名称.
解答 解:(1)已知0.5mol此有机物的质量为30g,该有机物的摩尔质量为:M=$\frac{30g}{0.5mol}$=60g/mol,
6g有机物的物质的量为:n(有机物)=$\frac{6g}{60g/mol}$=0.1mol,
3.6gH2O中H原子的物质的量为:n(H)=$\frac{3.6g}{18g/mol}$×2=0.4mol,
标况下4.48LCO2的物质的量为:n(CO2)=$\frac{4.48L}{22.4L/mol}$=0.2mol,n(C)=0.2mol,
根据质量守恒可知:12g有机物中:m(C)+m(H)=0.2mol×12g/mol+0.4mol×1g/mol=2.8g<6g,
故有机物中含有氧原子的质量为:m(O)=6g-2.8g=3.2g,
则氧原子的物质的量为:n(O)=$\frac{3.2g}{16g/mol}$=0.2mol,
所以:n(C):n(H):n(O)=0.2mol:0.4mol:0.2mol=1:2:1,
该有机物的最简式为:CH2O,分子式为(CH2O)n,又因相对分子质量为60,
即:30n=60,解得:n=2.
所以该有机物的分子式为:C2H4O2,
答:该有机物的分子式为C2H4O2;
(2)分子式为C2H4O2的有机物可能的结构简式为:CH3COOH、HCOOCH3、CH2(OH)CHO,
答:该有机物可能的结构简式为CH3COOH、HCOOCH3、CH2(OH)CHO;
(3)该物质能使石蕊试液变红,显酸性,其分子中含有羧基,其结构简式为:CH3COOH,为乙酸,
答:该有机物为乙酸,其结构简式为CH3COOH.
点评 本题考查有机物分子式、结构简式的确定,题目难度中等,注意掌握质量守恒定律在确定有机物分子式中的应用方法,明确常见有机物结构与性质为解答关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 温度一定时,当溶液中c(Ba2+)×c(SO42-)=1.07×10-10时,此溶液为BaSO4的饱和溶液 | |
| B. | 因为Ksp(BaCO3)>Ksp(BaSO4),所以无法将BaSO4转化为BaCO3 | |
| C. | 25℃时,在未溶解完BaCO3的饱和溶液中滴入少量Na2SO4溶液后有BaSO4沉淀析出,此时溶液中c(CO32-):c(SO42-)=24.11 | |
| D. | 在饱和BaCO3溶液中加入少量Na2CO3固体,可使c(Ba2+)减小,BaCO3的溶度积不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol${\;}_{8}^{16}$OD- 中含有的质子数、中子数均为9NA | |
| B. | 3.6 g石墨和C60的混合物中,含有的碳原子数为0.3NA | |
| C. | 反应3H2(g)+N2(g)?2NH3(g)△H=-92kJ/mol放出热量9.2kJ时,转移电子0.6NA | |
| D. | 标准状况下,4.48L戊烷含有的分子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用硫酸清洗锅炉中的水垢 | |
| B. | 溶液是电中性的,胶体是带电的 | |
| C. | 利用丁达尔效应可以区别溶液与胶体 | |
| D. | 烧碱、冰醋酸、四氯化碳均为电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MERS病毒疫苗的研制 | B. | 朝鲜的原子弹爆炸实验 | ||
| C. | 近期出现雾霾的原因探究 | D. | 马鞍山钢铁厂冶炼特种钢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 参数 | 比较 | 解释 |
| A | 沸点 | HF<HCl<HI | 组成结构相似的物质,相对分子质量越大沸点越高 |
| B | 半径 | Na+<Mg2+<Al3+ | 同一周期粒子半径随原子序数的递增逐渐减小 |
| C | 酸性 | H2SO3>H2CO3 | 元素的非金属性越强,其含氧酸的酸性越强 |
| D | 还原性 | P3->S2->Cl- | 元素的非金属性越强,简单阴离子的还原性越弱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
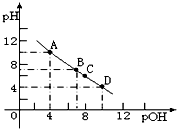 常温时,将氨气溶于水形成一浓度为0.1mol/L,pH为10的氨水溶液100mL.
常温时,将氨气溶于水形成一浓度为0.1mol/L,pH为10的氨水溶液100mL.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水高温条件下不易分解,是因为水分子内的H-O稳定 | |
| B. | 互为同分异构体的物质性质一定相似 | |
| C. | 分子组成若干个“CH12”原子团的有机化合物互称为同系物 | |
| D. | 因为互为同位素的核素的性质完全相同,所以这些核素在元素周期表中占据相同位置 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com