
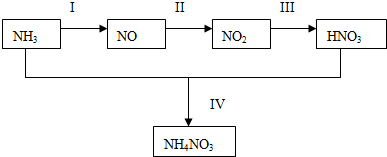
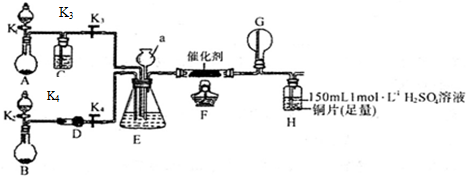
���� NH3��һϵ�з�Ӧ�õ�HNO3��NH4NO3�Ĺ��̣������Ĵ���������һ��������һ�������Ϳ�����������Ӧ���ɶ���������������������ˮ���������һ�����������������ᷴӦ��������泥�װ��ͼ��A��B�ֱ������Ʊ������Ͱ�������װ�ÿ�֪AӦ�����Ʊ�������CΪ����װ�ã���ΪŨ���ᣬBΪ�Ʊ�����װ�ã�����Ũ��ˮ��NaOH�����Ʊ���DΪ���ﰱ��װ�ã���F�з���������ԭ��Ӧ����NO��G�п����ɶ����������壬����������ˮ��H�з�Ӧ�������ᣬ������ͭ�����ɵ�NO����ֱ���ŷŵ������У�Ӧ��β������װ�ã�
����װ��ͼ��֪װ��A�����Ʊ����������ɹ��������ڶ������̴��������Ʊ���E�����ڻ���������Ͱ���������������ˮ��ע�ⲻ����ˮ��Һ��
�ڳɹ�ģ���˹��̢�ķ�Ӧ��˵�����ɶ����������壬��ɫΪ����ɫ��H�е���Һ�����ɫ��˵����������ͭ����ͭ���ӣ���ʹHװ����������ҺΪ������CuSO4��Һ��������������ʵ�����ȷ����������ͭ�����ʵ��������Nԭ���غ����������������ʵ������������㰱�������ʵ����������
��3��ʹG��Բ����ƿ�в����������̣�Ӧͨ�백�������ᷴӦ��
��4��װ��ȱ��β��������
��� �⣺װ��ͼ��A��B�ֱ������Ʊ������Ͱ�������װ�ÿ�֪AӦ�����Ʊ�������CΪ����װ�ã���ΪŨ���ᣬBΪ�Ʊ�����װ�ã�����Ũ��ˮ��NaOH�����Ʊ���DΪ���ﰱ��װ�ã���F�з���������ԭ��Ӧ����NO��G�п����ɶ����������壬����������ˮ��H�з�Ӧ�������ᣬ������ͭ�����ɵ�NO����ֱ���ŷŵ������У�Ӧ��β������װ�ã�
����װ��ͼ��֪װ��A�����Ʊ����������ɹ��������ڶ������̴��������Ʊ�����Ӧ�ķ���ʽΪ2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2����E�����ڻ���������Ͱ���������ͨ�백��������������ȡ�ƽ��װ���ڵ�ѹǿ������������ˮ��������ˮ��Һ����d����
�ʴ�Ϊ��2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2����d��
�ڳɹ�ģ���˹��̢�ķ�Ӧ��˵�����ɶ����������壬��ɫΪ����ɫ��H�е���Һ�����ɫ��˵����������ͭ����ͭ���ӣ���Ӧ�����ӷ���ʽΪ3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��n��H2SO4��=0.15L��1mol/L=0.15mol����n��CuSO4��=0.15mol����Ҫ0.15molCu������3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��֪��Ҫ0.1molHNO3����Nԭ���غ��֪��Ҫ0.1mol���������Ϊ0.1mol��22.4L/mol=2.24L��
�ʴ�Ϊ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��2.24L��
��3��ʹG��Բ����ƿ�в����������̣�Ӧͨ�백�������ᷴӦ����A�Ʊ�������B�Ʊ���������ر�K3��Ϩ��ƾ��ƣ��ʴ�Ϊ��a��
��4��������ɵ�NO����ֱ���ŷŵ������У�Ϊ��ֹ��Ⱦ������Ӧ��β������װ�ã��ʴ�Ϊ��ȱ��β������װ�ã�
���� ���⿼���˰����Ʊ�����ѧ���ʣ�Ϊ�߿��������ͣ���Ŀ�Ѷ��еȣ�ע�����հ������Ʊ�ԭ�������еĻ�ѧ���ʣ����������Ϣ��ȷʵ��Ŀ�ļ���Ӧԭ��Ϊ���ؼ�����������������ѧ���ķ�����������������ѧʵ��������


 ����5��2���ϵ�д�
����5��2���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
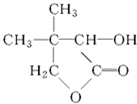 G�ĺϳ�·����ͼ��
G�ĺϳ�·����ͼ��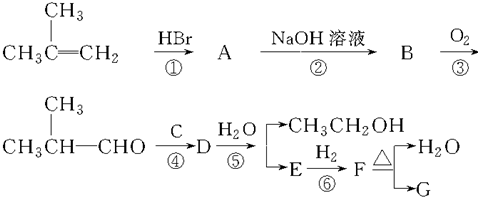
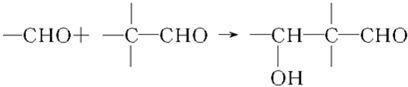
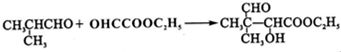
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ˮ�����ԣ����Զ��������������������� | |
| B�� | ������������������������������ | |
| C�� | ������̼ͨ��ˮ�������Եõ����� | |
| D�� | ��Ϊ����ʱ����������̼���Ʒ�Ӧ�ų�������̼�����Թ�������Ա�̼��ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
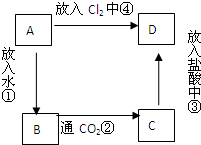 ����A����AԪ����ɵĵ��ʣ������ھƾ��ƻ��������գ�����Ϊ��ɫ��B��C��D�Ǻ���AԪ�ص����ֲ�ͬ�����A��B��C��D��ͼ��ϵ����ת����
����A����AԪ����ɵĵ��ʣ������ھƾ��ƻ��������գ�����Ϊ��ɫ��B��C��D�Ǻ���AԪ�ص����ֲ�ͬ�����A��B��C��D��ͼ��ϵ����ת�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | CH3COOH | H2CO3 | HNO2 |
| ���볣�� | K=1.8��10-5 | K=4.3��10-7 K=5.6��10-11 | K=5.0��10-4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ԭ����HCl����������MnO2 | |
| B�� | ÿ����1mol MnO2��ת�Ƶ��ӵ����ʵ���Ϊ2 mol | |
| C�� | ÿת��1mol���ӣ�������Ƶñ����Cl2 22.4L | |
| D�� | ���ɵ�Cl2�У�������һЩˮ�����⣬������HCl���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com