
【题目】颠茄酸酯(J)是一种溃疡病治疗的辅助药物,其合成路线如下,回答下列问题:

(1) 烃B的相对分子质量为104,分子中氢的质量分数为7.69%,且反应①为加成反应,则X含有的官能团的名称是_______________,物质B的名称为_______________。
(2) 反应③的反应类型为_______________。
(3) C的结构简式为_________________________。
(4) 写出D→E反应的化学方程式_____________________________________________。
(5) 化合物I有多种同分异构体,同时满足下列条件的结构有_________种。
①能发生水解反应和银镜反应;
②能与FeCl3发生显色反应;
③苯环上有四个取代基,且苯环上一卤代物只有一种。
其中某种同分异构体进行水解反应时,1mol该物质消耗3molNaOH,该同分异构体的结构简式为____________________。(写出一种即可)
【答案】碳碳三键 苯乙烯 消去反应 ![]() 2
2![]() +O2
+O2![]() 2
2![]() +2H2O 6
+2H2O 6  或
或 
【解析】
由烃B中含氢的质量分数为7.69%,B的相对分子质量为104,所以含有H原子数为:104![]() 7.69%=8,含碳原子数为:
7.69%=8,含碳原子数为:![]() =8,所以烃B的分子式为C8H8。反应①为加成反应,所以X为CH
=8,所以烃B的分子式为C8H8。反应①为加成反应,所以X为CH![]() CH,和苯发生加成反应生成B
CH,和苯发生加成反应生成B![]() 。
。![]() 与HBr发生加成反应生成C,所以C为卤代烃,C在NaOH溶液中发生水解生成醇D,醇在铜催化下加热发生催化氧化生成醛或酮E,E能和新制的氢氧化铜反应,所以B和HBr加成时,溴原子加在端点碳原子上,所以C的结构简式为:
与HBr发生加成反应生成C,所以C为卤代烃,C在NaOH溶液中发生水解生成醇D,醇在铜催化下加热发生催化氧化生成醛或酮E,E能和新制的氢氧化铜反应,所以B和HBr加成时,溴原子加在端点碳原子上,所以C的结构简式为:![]() 。C发生卤代烃的水解反应生成D(
。C发生卤代烃的水解反应生成D(![]() ),D催化氧化生成E(
),D催化氧化生成E(![]() ),E和新制的氢氧化铜反应后酸化生成F(
),E和新制的氢氧化铜反应后酸化生成F(![]() ), F与乙醇发生酯化反应生成G为
), F与乙醇发生酯化反应生成G为![]() ,结合有机物H的结构可知反应②发生取代反应,同时生成乙醇。H与氢气发生加成反应生成I为
,结合有机物H的结构可知反应②发生取代反应,同时生成乙醇。H与氢气发生加成反应生成I为 反应③是I在浓硫酸、加热条件下发生消去反应生成J(颠茄酸酯);
反应③是I在浓硫酸、加热条件下发生消去反应生成J(颠茄酸酯); 。
。
(1)由烃B中含氢的质量分数为7.69%,B的相对分子质量为104,所以含有H原子数为:104![]() 7.69%=8,含碳原子数为:
7.69%=8,含碳原子数为:![]() =8,所以烃B的分子式为C8H8。反应①为加成反应,所以X为CH
=8,所以烃B的分子式为C8H8。反应①为加成反应,所以X为CH![]() CH,和苯发生加成反应生成B
CH,和苯发生加成反应生成B![]() ,名称为苯乙烯。X为C2H2,X分子中含有碳碳三键;
,名称为苯乙烯。X为C2H2,X分子中含有碳碳三键;
答案:碳碳三键;苯乙烯;
(2) 反应③是I在浓硫酸、加热条件下发生消去反应生成J: ,所以反应③的反应类型为消去反应;答案:消去反应;
,所以反应③的反应类型为消去反应;答案:消去反应;
(3)根据分析可知: B与HBr发生加成反应生成C,所以C的结构简式为:![]() ;答案:
;答案:![]() 。
。
(4)由上述分析可知D为![]() ,在根据框图
,在根据框图 ![]() 可知,D→E发生氧化反应,反应的化学方程式:2
可知,D→E发生氧化反应,反应的化学方程式:2![]() +O2
+O2![]() 2
2![]() +2H2O;答案:2
+2H2O;答案:2![]() +O2
+O2![]() 2
2![]() +2H2O。
+2H2O。
(5) 通过分析可知化合物I的结构简式为: ,有多种同分异构体,同时满足(1)能发生水解和银镜反应,所以含有酯基和醛基,I的苯环上连接的基团只有一个不饱和度,所以酯基和醛基要合二为一,即必须为甲酸酯;(2)能与FeCl3发生显色反应,说明含有酚羟基,(3)苯环上有四个取代基,且苯环上一卤代物只有一种说明苯环上含有一种氢原子,其结构简式为:
,有多种同分异构体,同时满足(1)能发生水解和银镜反应,所以含有酯基和醛基,I的苯环上连接的基团只有一个不饱和度,所以酯基和醛基要合二为一,即必须为甲酸酯;(2)能与FeCl3发生显色反应,说明含有酚羟基,(3)苯环上有四个取代基,且苯环上一卤代物只有一种说明苯环上含有一种氢原子,其结构简式为: ,
, ,
, ,
, ,
, ,
, 共6种;其中某种同分异构体进行水解反应时,1mol该物质消耗3molNaOH,该同分异构体的结构简式为:
共6种;其中某种同分异构体进行水解反应时,1mol该物质消耗3molNaOH,该同分异构体的结构简式为: ,
, ;答案:6 ;
;答案:6 ;  或
或  。
。


科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g) ![]() C(g) +D(g) 发生过程中的能量变化如图,△H 表示反应的焓变。下列说法正确的是( )
C(g) +D(g) 发生过程中的能量变化如图,△H 表示反应的焓变。下列说法正确的是( )
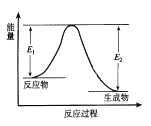
A. 反应体系中加入催化剂,反应速率增大,E1减小,E2增大
B. 反应体系中加入催化剂,反应速率增大,△H增大
C. △H < 0,反应达到平衡时,升高温度,A的转化率减少
D. △H > 0,反应达到平衡时,增大压强,A的转化率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍![]() 、铁作电极电解浓NaOH溶液制备高铁酸盐
、铁作电极电解浓NaOH溶液制备高铁酸盐![]() 的装里如图所示。下列推断合理的是
的装里如图所示。下列推断合理的是
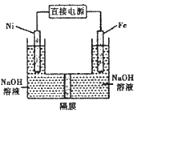
A.镍是阳极,电极反应为![]()
B.电解时电流的方向为:负极![]() 电极
电极![]() 溶液
溶液![]() 电极
电极![]() 正极
正极
C.若隔膜为阴离子交换膜,则![]() 自左向右移动
自左向右移动
D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH升高![]() 假设电解前后体积变化忽略不计
假设电解前后体积变化忽略不计![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是工业上采用离子交换膜法电解足量饱和食盐水的示意图。下列有关说法中不正确的是( )

A.从E口逸出的是氢气
B.向B口中加入含少量NaOH的溶液以增强导电性
C.标准状况下每生成22.4 L Cl2,便产生2 mol NaOH
D.向电解后的阳极室溶液中加入适量盐酸,各物质可以恢复到电解前的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,将![]() 通入足量水中,生成
通入足量水中,生成![]() 的分子数为
的分子数为![]()
B.铁与稀硝酸反应生成的气体产物仅有![]() ,转移的电子数一定为
,转移的电子数一定为![]()
C.15g乙烷与1mol氯气充分反应,所得有机物中含有的氯原子数为![]()
D.![]() 中含有的质子数和中子数均为
中含有的质子数和中子数均为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是![]()
![]()
A.![]() 的乙醇溶液中,含
的乙醇溶液中,含![]() 键的数目为
键的数目为![]()
B.标准状况下,![]() 乙炔和苯的混合物中含
乙炔和苯的混合物中含![]() 键数目为
键数目为![]()
C.![]() 溶液中含
溶液中含![]() 数目为
数目为![]()
D.某温度下,![]() 的
的![]() 溶液中,水电离出的
溶液中,水电离出的![]() 总数为
总数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
A. 2H2(g)+O2(g) == 2H2O(1) △H= ―285.8kJ/mol![]()
B. 2H2(g)+ O2(g) == 2H2O(1) △H= +571.6 kJ/mol
C. 2H2(g)+O2(g) == 2H2O(g) △H= ―571.6 kJ/mol
D. H2(g)+1/2O2(g) == H2O(1) △H= ―285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盖斯定律在生产和科学研究中有很重要的意义。已知3.6g碳在6.4g氧气中燃烧,至反应物耗尽,放出了X kJ热量。已知碳完全燃烧的焓变△H= 一Y kJ·mol-1,则lmol C与O2反应生成CO的反应热△H为 ( ) kJ·mol-1
A.一Y B.—(10X—Y) C.一(5X—O.5Y) D.+(10X—Y)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向10 mL 0.1 mol/LCuCl2溶液中滴加0.1 mol/L的Na2S溶液,滴加过程中溶液中lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,已知:lg2=0.3,Ksp(ZnS)=3×10-25 。下列有关说法正确的是( )

A.a、b、c三点中,水的电离程度最大的为b点
B.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+)
C.该温度下Ksp(CuS)=4×10-36
D.向100 mL Zn2+、Cu2+浓度均为10-5 mol/L的混合溶液中逐滴加入10-4 mol/L的Na2S溶液,Zn2+先沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com