
分析 根据温度、浓度、催化剂、接触面积对反应速率的影响可知,降低温度,反应速率减慢,而增大接触面、使用催化剂、增大浓度加快反应速率.
解答 解:(1)食物保存在冰箱里是通过降低温度达到减慢失误腐败变质的反应速率的目的,故选D;
(2)H2O2分解时,少量的MnO2起到催化剂的作用,可以加快水分解的速率,故选B;
(3)大小相同是Mg与Al分别投入到相同浓度的盐酸中,Mg反应较快,是因为金属Mg的活泼性强于金属铝,即内因决定的,故选E;
(4)相同大小的锌片在3mol/L的H2SO4中比在1mol/L的H2SO4中反应快,是因为硫酸的浓度越大,反应速率越快,故选A;
(5)铁粉比铁片在同浓度的盐酸中反应快,是因为铁粉的表面积大于铁片,故选C.
点评 本题考查影响反应速率的因素,熟悉温度、浓度、催化剂、接触面积对反应速率的影响即可解答,题目难度不大.


科目:高中化学 来源: 题型:填空题
| 元素代号 | A | B | C | D | E | F | G | H |
| 原子半径/pm | 37 | 160 | 70 | 66 | 186 | 143 | 104 | 99 |
| 最高化合价 | +1 | +2 | +5 | +1 | +3 | +6 | +7 | |
| 最低化合价 | -3 | -2 | -2 | -1 |
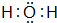 ,B、H两种元素形成化合物的电子式是
,B、H两种元素形成化合物的电子式是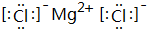 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10s-15sC(NH3)增加量等于0.25 mol/L | |
| B. | 化学反应速率的关系是3v正(H2)=2v正(NH3) | |
| C. | 达到平衡后,分离出少量NH3,平衡正向移动,v正增大 | |
| D. | 保持压强不变充入Ar气体,v正减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素编号 | ① | ② | ② | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 |
| A. | ⑦①可形成离子化合物 | |
| B. | 元素②⑥形成的化合物具有两性 | |
| C. | 元素②氢化物的沸点小于元素⑤氢化物的沸点 | |
| D. | 元素④气态氢化物的稳定性大于元素⑤气态氢化物的稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
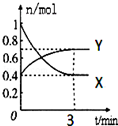 在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)?N2O4(g)(无色),如图所示.
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)?N2O4(g)(无色),如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 青蒿素属于烃 | B. | 青蒿素属于烷烃 | ||
| C. | 青蒿素属于无机化合物 | D. | 青蒿素属于有机化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 压强/MPa | ||||
| SO2平衡 | ||||
| 转化率/% | ||||
| 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
| A. | 0.1 MPa,400℃ | B. | 0.5 MPa,500℃ | C. | 1 MPa,600℃ | D. | 10 MPa,600℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com