
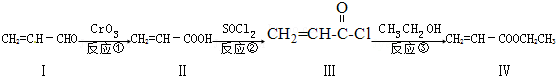
 ��ע����Ӧ��������
��ע����Ӧ�������� ��CH2=CH-O-CH2-O-CH=CH2��
��CH2=CH-O-CH2-O-CH=CH2�� Ҳ���뻯����������Ʒ�Ӧ�۵ķ�Ӧ����õ��IJ���Ľṹ��ʽΪ
Ҳ���뻯����������Ʒ�Ӧ�۵ķ�Ӧ����õ��IJ���Ľṹ��ʽΪ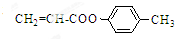 ��
�� ���� ��1���Ƚ�CH2=CH-COOH��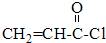 �Ľṹ��֪��Ӧ�ڵķ�Ӧ���ͣ����ݻ�������Ľṹ��ʽ�ɵ÷���ʽ��д����Ӧ�ķ���ʽ�ɵú�������
�Ľṹ��֪��Ӧ�ڵķ�Ӧ���ͣ����ݻ�������Ľṹ��ʽ�ɵ÷���ʽ��д����Ӧ�ķ���ʽ�ɵú�������
��2��������II�еĹ�������̼̼˫�����Ȼ�������̼̼˫��������Է����ӳɷ�Ӧ��
��3���ȽϢ�͢�ṹ��֪��Ӧ���ͣ�����������ȩ����Ϣ��ķ���ʽ�͢�Ľṹ��ʽ����֪��Ϊϩ�����ɴ˿�д����������ȩ�ķ���ʽ��
��4������CH2=CH-COOCH2CH3�Ľṹ��֪�����IJ����Ͷ�Ϊ2�����Ǣ���һ����֧����ͬ���칹�壬��̼�����˳ʶԳƽṹ�����Ԣ���Ӧ������̼̼˫����̼��˫������5����Ӧ��ԭ���ǽṹ����ԭ�ӱ�����������ȡ�������д�����������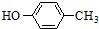 ��Ӧ�IJ��
��Ӧ�IJ��
��� �⣺��1���Ƚ�CH2=CH-COOH��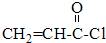 �Ľṹ��֪��Ӧ�ڵķ�Ӧ����Ϊȡ����Ӧ���������ĺ���������ȼ��ͨʽ�ɵã�C5H8O2+6O2 $\stackrel{��ȼ}{��}$5CO2+4H2O������������������ʵ���֮�ȵ���ϵ��֮�ȣ���1mol����ȫȼ��������Ҫ����6mol O2��
�Ľṹ��֪��Ӧ�ڵķ�Ӧ����Ϊȡ����Ӧ���������ĺ���������ȼ��ͨʽ�ɵã�C5H8O2+6O2 $\stackrel{��ȼ}{��}$5CO2+4H2O������������������ʵ���֮�ȵ���ϵ��֮�ȣ���1mol����ȫȼ��������Ҫ����6mol O2��
�ʴ�Ϊ��ȡ����6��
��2��������II�еĹ�������̼̼˫�����Ȼ�������̼̼˫��������Է����ӳɷ�Ӧ����Ӧ����ʽΪ��CH2=CHCOOH+Br2��CH2BrCHBrCOOH��
�ʴ�Ϊ��̼̼˫�����Ȼ���CH2=CHCOOH+Br2��CH2BrCHBrCOOH��
��3������������ȩ����Ϣ��ķ���ʽ�͢�Ľṹ��ʽ����֪��Ϊϩ�����ṹ��ʽΪ��CH2=CH-CH2OH���ɴ˿�д����������ȩ�ķ���ʽ�� ��
��
�ʴ�Ϊ�� ��
��
��4������CH2=CH-COOCH2CH3�Ľṹ��֪�����IJ����Ͷ�Ϊ2�����Ǣ���һ����֧����ͬ���칹�壬��̼�����˳ʶԳƽṹ�����Ԣ���Ӧ������̼̼˫����̼��˫�������Ԣ��Ľṹ��ʽΪOHCCH2CH2CH2CHO �� ��CH2=CH-O-CH2-O-CH=CH2��
��CH2=CH-O-CH2-O-CH=CH2��
�ʴ�Ϊ��OHCCH2CH2CH2CHO �� ��CH2=CH-O-CH2-O-CH=CH2��
��CH2=CH-O-CH2-O-CH=CH2��
��5����Ӧ��ԭ���ǽṹ����ԭ�ӱ�����������ȡ�������д����������� ��Ӧ�IJ���Ϊ��
��Ӧ�IJ���Ϊ��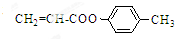 ��
��
�ʴ�Ϊ��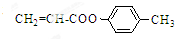 ��
��
���� �������л���ĺϳɿ���ṹ�����ʣ������л�����ʹ��������ɺ������Լ��������ϵ����Ҫ�л���Ӧ������ȡ����Ӧ���ӳɷ�Ӧ����ȥ��Ӧ��������Ӧ��Ϊ���Ĺؼ����ۺϿ��鿼���ķ����������������������ۺ�Ӧ����Ϣ�Լ���ϢǨ��������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
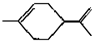 �������й������Ʋⲻ��ȷ���ǣ�������
�������й������Ʋⲻ��ȷ���ǣ�������| A�� | ������ʹ���Ը��������Һ��ɫ | |
| B�� | ������ΪҺ̬��������ˮ | |
| C�� | ����ʽΪC10H16 | |
| D�� | ����������CCl4��Һ��Ӧ�����Ϊ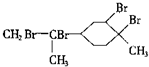 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ ˮú�� ���� �ɱ� | |
| B�� | ����ˮ ������Һ ������ �������� | |
| C�� | ���� ������ �� ̼��� | |
| D�� | �ظ� �ո� �Ȼ�ͭ ̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij�¶��£���2L�ܱ������У�����NO2��N2O4֮��ķ�Ӧ��N2O4��g��?2NO2��g���������ʵ�����ʱ��ı仯��ϵ��ͼ��ʾ����ش��������⣮
ij�¶��£���2L�ܱ������У�����NO2��N2O4֮��ķ�Ӧ��N2O4��g��?2NO2��g���������ʵ�����ʱ��ı仯��ϵ��ͼ��ʾ����ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��30 mL 1 mol/L Na2SO3��Һ��ͨ���״���µ�Cl2 224 mL��H2O+SO${\;}_{3}^{2-}$+Cl2�TSO${\;}_{4}^{2-}$+2Cl-+2H+ | |
| B�� | ��������Һ�еμӹ�����ˮ��Ag++2NH3•H2O�T[Ag��NH3��2]++2H2O | |
| C�� | ����̼������Һ��ͨ�������̼����Һ����ǣ�2Na++CO32-+CO2+H2O�T2NaHCO3�� | |
| D�� | ̼����þ��Һ�м��������ij���ʯ��ˮ��Mg2++2HCO3-+2Ca2++4OH-�TMg��OH��2��+2CaCO3��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | Ԫ�� | C�� | ���� | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com