
| A�� | �÷�Ӧ�ﵽƽ��״̬ | |
| B�� | �÷�Ӧ�������淴Ӧ������� | |
| C�� | ��ƽ��״̬ʱ��H2��ת����ӦΪ96.3% | |
| D�� | ����H2�������÷�Ӧƽ�ⳣ������С |
���� ��ﵽƽ��ʱת��������Ϊx����
H2��g��+I2��g��?2HI��g��
��ʼ 0.4 1 0
ת�� x x 2x
ƽ�� 0.4-x 1-x 2x
$\frac{��2x��^{2}}{��0.4-x����1-x��}$=64��x=0.3582mol/L��
ƽ��ʱ������ת����Ϊ$\frac{0.3582}{0.4}$��100%=96.3%��
���K���¶��й������
��� �⣺��ﵽƽ��ʱת��������Ϊx����
H2��g��+I2��g��?2HI��g��
��ʼ 0.4 1 0
ת�� x x 2x
ƽ�� 0.4-x 1-x 2x
$\frac{��2x��^{2}}{��0.4-x����1-x��}$=64��x=0.3582mol/L��
ƽ��ʱ������ת����Ϊ$\frac{0.3582}{0.4}$��100%=96.3%��
A��H2ת����Ϊ50%ʱ��С��ƽ��ʱת����Ϊ96.3%����֪��Ӧ������Ӧ�����ƶ�����A����
B����ѡ��A��֪���÷�Ӧ����������Ӧ������У���B����
C�������������֪��ƽ��״̬ʱ��H2��ת����Ϊ96.3%����C��ȷ��
D��K���¶��йأ��¶Ȳ��䣬����H2�������÷�Ӧƽ�ⳣ�������䣬��D����
��ѡC��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬���ջ�ѧƽ�����η���K��ת���ʵļ���Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��ѡ��DΪ�״��㣬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���븴ԭ�����ķ�Ӧ����Ϊ��3Ag2S+2Al=6Ag+Al2S3 | |
| B�� | ��������ʱ��������������ж� | |
| C�� | �����鶾ʱ��Ag������ | |
| D�� | �����鶾��Ӧ����������ͻ�ԭ��������ʵ���֮��Ϊ1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ҵ���Ũ����ֱ���170���140��������·�Ӧ | |
| B�� | ������ֱ���NaOH��ˮ��Һ��NaOH�Ĵ���Һ�з�Ӧ | |
| C�� | ����ϩ�ƾ�����ϩ�����ᣨ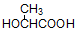 ���ϳɾ����� ���ϳɾ����� | |
| D�� | �Ҵ�ʹ�����ظ������Һ��ɫ����ȩ������������ͭ����Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��NaCl�����У���Na+�����Cl-�γ��������� | |
| B�� | 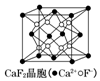 ��CaF2�����У�ÿ������ƽ��ռ��4��Ca2+ | |
| C�� | 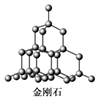 �ڽ��ʯ�����У�6��̼ԭ���γ�һ�����Ҳ���ͬһƽ���� | |
| D�� |  ����̬�Ŵط��ӵķ���ʽΪEF��FE |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2��Cl2 | B�� | H2��O2 | C�� | H2��Br2 | D�� | H2��F2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com