
分析 根据分子的空间构型分析,正四面体的键角为109°28′,三角锥形的键角为107°,V形的键角为105°,据此分析.
解答 解:(a)CH4的空间构型为正四面体,中心原子没有孤电子对,其键角为109°28′,NH3的空间构型为三角锥,中心原子含有1个孤电子对,孤对电子对成键电子的排斥作用较强,键角减小,其键角为107°,
答:CH4的键角大;甲烷中没有孤电子对,孤对电子对成键电子的排斥作用较强;
(b)OF2和Cl2O的空间构型均为V形,中心原子含有2个孤电子对,孤对电子对成键电子的排斥作用较强,键角减小,其键角为105°,
答:二者的键角相同;OF2和Cl2O的空间构型均为V形,键角为105°;
(c)NH3和NF3的空间构型为三角锥,中心原子含有2个孤电子对,孤对电子对成键电子的排斥作用较强,键角减小,其键角为107°,
答:二者的键角相同;NH3和NF3的空间构型为三角锥,键角为107°;
(d)PH3和NH3的空间构型为三角锥,中心原子含有2个孤电子对,孤对电子对成键电子的排斥作用较强,键角减小,其键角为107°,
答:二者的键角相同;PH3和NH3的空间构型为三角锥,键角为107°.
点评 本题考查了键角、分子的空间构型,题目难度中等,明确孤对电子对成键电子的排斥作用较强是解题的关键.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 该反应中次磷酸根离子得电子,表现还原性 | |
| B. | 该反应中氧化剂与还原剂的物质的量之比为1:1 | |
| C. | 该反应每消耗3 molX,转移电子的物质的量为2mol | |
| D. | 若将硫酸铜溶液换成硝酸银溶液,容器内壁不会形成镀层 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
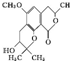
| A. | 每个分子中有2个手性碳原子 | |
| B. | 能与FeCl3溶液发生显色反应 | |
| C. | 1 mol该物质最多可与含2 mol NaOH的水溶液反应 | |
| D. | 分子中有3种含氧官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.00 | B. | 1.00 | C. | 0.7 | D. | 1.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用海水不经化学变化即可制得食盐和淡水 | |
| B. | 在新装修的居室里放置数盆清水,可有效地吸收房间中释放的甲醛、苯等有害气体 | |
| C. | 等质量的乙烯和聚乙烯燃烧时,聚乙烯产生的二氧化碳多 | |
| D. | 石油分馏可获得乙酸、苯等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 苹果汁的c(H+)=0.3mol•L-1 | B. | 生理盐水是一种中性溶液 | ||
| C. | 石灰水的碱性比肥皂水强 | D. | 石灰水与苹果汁能发生中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| O2 | Na2CO3 | CO2 | 转移电子数 | |
| A | 1mol | 0.5NA | ||
| B | 0.5mol | 11.2L | ||
| C | 0.25mol | 53g | ||
| D | 8g | NA |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Bi元素的质量数是209 | |
| B. | Bi元素最高价氧化物的化学式为Bi2O3 | |
| C. | Bi元素位于元素周期表第六周期第VA族 | |
| D. | Bi为放射性元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com