
�Ƽ��仯������й㷺����;��
��1����ҵ���Ʊ������Ƶij��÷�����_______����д���Ʊ������ƵĻ�ѧ����ʽ_____________�������ƿ�����________________��д��Na���۵�ͷ����һ����;����
��2����Na2CO3������������ʣ�CO��O2��CO2Ϊԭ�Ͽ�������͵�ء��õ�صĽṹ��ͼ��ʾ��

�������ĵ缫��ӦʽΪ_______����ع���ʱ����A��ѭ��ʹ�ã�A���ʵĻ�ѧʽΪ_______��
����д������Na2CO3����Ԫ�صķ���_________________________��
��3�������£�Ũ�Ⱦ�Ϊ0.1 mol��L��1����������������Һ��pH���±���
���� | CH3COONa | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 11.6 | 10.3 | 11.1 |
��������Һ���������У����H��������ǿ����_________�����ݱ������ݣ�Ũ�Ⱦ�Ϊ0.01 mol��L��1���������������Һ�ֱ�ϡ��100����pH�仯������_______������ţ���
a��HCN b��HClO c��CH3COOH d��H2CO3
��4��ʵ�����г���NaOH������β��������ϴ�����ᴿ��
�ٳ����£���300 mL 1 mol��L��1��NaOH��Һ����4.48 L������ɱ�״����SO2ʱ��������ҺpH>7������Һ�и�����Ũ���ɴ�С��˳��Ϊ_______��
����֪�������ӿ�ʼ����ʱ��pH���±���
���� | Fe2�� | Cu2�� | Mg2�� |
pH | 7.6 | 5.2 | 10.4 |
������ͬŨ��Cu2����Mg2����Fe2������Һ�еμ�ijŨ�ȵ�NaOH��Һʱ��_______�������ӷ��ţ��ȳ�����Ksp_______Ksp�����������������������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ʡ��ɳ��2016-2017ѧ���һ��ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ�ѡ����
������Һ�е����ӡ����ܴ����������
A. ������ MnO4-����Һ�У�Na+��K+��Cu2+��Fe3+
B. �ڼ��������ܲ�����������Һ�У�NH4+��Fe2+��SO42-��NO3-
C. ������Һ�У�Ba2+��NO3-��K+��AlO2-
D. ������ Fe3+����Һ�У�NH4+��Na+��I-��SCN-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ�����е���У�����ڶ������Ͽ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
һ�������£�������ͼװ�ÿ�ʵ���л���Ĵ��⣬�����й�˵����ȷ����(����)

A. ���ڵ缫D�ŵ�ʱ�Ͽ��Ļ�ѧ���Ǽ��Լ�
B. ����X�ڷ�Ӧ��ͨ�����ֻ�ԭ��
C. ���������ĵ������ҺΪϡ���ᣬ����һ��ʱ�����������Һ��pH����
D. �缫D�ĵ缫��ӦʽΪC6H6��6H����6e��===C6H12
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�ϲ��и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����л����к��У� ���ֹ�����
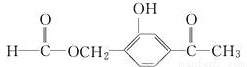
A. 1 B. 2 C. 3 D. 4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�ϲ��и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ˮ��Ϻ��ã������ֲַ����
A. �� B. �Ҵ� C. �ȷ� D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��㶫ʡ�����и߶���ѧ�ڵ�һ���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ���ܴﵽʵ��Ŀ���ҷ���ʵ�����Ҫ����ǣ� ��
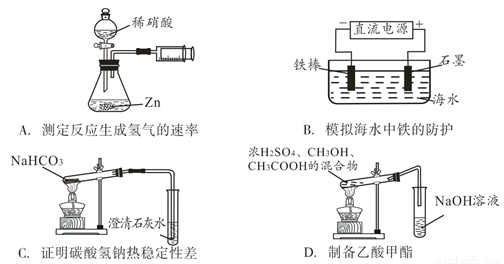
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ���ٴ�һ�и���1���������ۻ�ѧ�Ծ��������棩 ���ͣ������
̼���������CH3OCOOCH3�����DMC������һ��Ӧ��ǰ���㷺���²��ϣ�ʵ�����п��ü״���CO��CO2�Ƚ��кϳɡ��ش��������⣺
��1��������̼�ĵ���ʽΪ _________________
��2���ü״���CO��O2�ڳ�ѹ��70��120��ʹ����������ºϳ�DMC��
��֪����CO�ı�ȼ����Ϊ��?283.0kJ•mol?1��
��1mol H2O��l����ȫ�������H2O��g��������44kJ������
��2CH3OH��g����CO2��g��?CH3OCOOCH3��g����H2O��g����H��?15.5kJ•mol?1
��2CH3OH��g����CO��g����1/2O2��g��?CH3OCOOCH3 ��g����H2O��l����H��_____��
�÷�Ӧ�ڳ�ѹ��70��120�������¾����Է���Ӧ��ԭ����_______________��
��3����������Ӧ��֪�״���CO2��ֱ�Ӻϳ�DMC���״�ת����ͨ�����ᳬ��1%����Լ�÷�Ӧ����ҵ��������
��д���÷�Ӧƽ�ⳣ������ʽ��______________ ��
���ں����ܱ������з���������Ӧ����˵���Ѵﵽƽ��״̬����____��ѡ���ţ���
A��v����CH3OH����2v�棨CO2��
B��CH3OCOOCH3��H2O�����ʵ���֮�ȱ��ֲ���
C��������������ܶȲ���D��������ѹǿ����
��ij�о�С����ij�¶��£���100mL�����ܱ�������Ͷ��2.5mol CH3OH��g��������CO2��6��10?5 mol�������о���Ӧʱ��Լ״�ת������TON����Ӱ�죬��仯������ͼ1��ʾ�������㹫ʽΪ��TON��ת���ļ״������ʵ���/���������ʵ�������
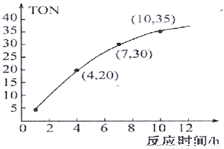
�ڸ��¶��£���ѷ�Ӧʱ����_________h��4��10h��DMC��ƽ����Ӧ������_______ ��
��4���Զ�ײ�Ϊ�缫��������ͼװ����A��B�ڷֱ�ͨ��CH3OCOOCH3��O2����ȼ�ϵ�أ���д���õ�ظ����ĵ缫��Ӧʽ____________________________
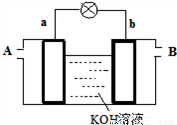
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ����ˮ����ѧ������У����2��������ѧ�Ծ��������棩 ���ͣ�ѡ����
25��ʱ��������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����
A. 0.1mol��L-1NaHC2O4��Һ��pH=5.5����c(Na+)> c(HC2O4-)> c(H2C2O4)> c(C2O42-)
B. 0.1mol��L-1NaHS��Һ��c(OH-)+ c(S2-)= c(H+)+ c(H2S)
C. 0.1mol��L-1CH3COOH��Һ��0.1mol��L-1CH3COONa��Һ�������ϣ�c(Na+)> c(CH3COOH)> c(CH3COO-)> c(H+)> c(OH-)
D. 0.1mol��L-1NH4HSO4��Һ�еμ�0.1mol��L-1NaOH��Һ�����ԣ�c(Na+)> c(SO42-)>c(NH4+)> c(OH-)= c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ̨���и�����ѧ����ĩ�����������Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£����ʵ���Ũ����ȵ��������ʵ�ˮ��Һ��pH��С����
A. NaOH B. FeCl3 C. Na2CO3 D. NaCl
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com