
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2molSO2、1molO2 | 1molSO2、0.5molO2 | 2molSO3 |
| k1 | k2 | k3 | |
| 反应的能量变化 | 放出akJ | 放出bkJ | 吸收ckJ |
| 气体密度 | ρ1 | ρ2 | ρ3 |
| 反应物转化率 | α1 | α2 | α3 |
| A. | k1=k3<k2 | B. | ρ1=ρ3>ρ2 | C. | α2+α3>1 | D. | 2b+c>197 |
分析 A.平衡常数随温度变化,不随浓度变化;
B.甲和丙分别是正向和逆向达到的平衡状态,保持恒温、恒容,最后得到相同平衡状态,气体体积不变,质量不变,乙起始量和甲相比少一半,气体质量为甲的一半;
C,甲和丙达到相同的平衡状态,正向和逆向得到相同的平衡状态,α1+α3=1,甲和乙相比甲中二氧化硫转化率大于乙中二氧化硫转化率;
D.甲投入2molSO2、1molO2,丙中投入2molSO3,则甲与丙是完全等效的,根据盖斯定律可知,甲与丙的反应的能量变化之和为197kJ,故a+c=197,起始量分析可知a=2b.
解答 解:A.平衡常数随温度变化,不随浓度变化,恒温、恒容条件下k1=k3=k2,故A错误;
B.保持恒温、恒容,甲和丙最后得到相同平衡状态,气体体积不变,质量不变,密度相同,乙起始量和甲相比少一半,气体质量为甲的一半密度为甲中的一半,ρ1=ρ3>ρ2,故B正确;
C,甲和丙达到相同的平衡状态,正向和逆向得到相同的平衡状态,α1+α3=1,甲和乙相比,甲相当于乙平衡状态下加入二氧化硫和氧气,有志气增大平衡正向进行,甲中二氧化硫转化率大于乙中二氧化硫转化率,2+α3<1,故C错误;
D.甲投入2molSO2、1molO2,丙中投入2molSO3,则甲与丙最后达到相同的平衡状态,平衡是完全等效的,根据盖斯定律可知,甲与丙的反应的能量变化之和为197kJ,故a+c=197,甲的起始量为乙的起始量2倍,则a>2b,2b+c<197,故D错误;
故选B.
点评 本题考查化学平衡影响因素、等效平衡、化学平衡的计算,题目计算量较大,题目难度较大,关键是构建平衡建立的等效途径,试题侧重对学生灵活运用基础知识解决实际问题的能力的培养.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石墨为阴极,阳极上有气体产生 | |
| B. | 铁作阳极,阴极的反应式为2H++2e-═H2 | |
| C. | 铁作阴极,阳极的反应式为2 MnO42--2e-═2 MnO4- | |
| D. | 石墨为阳极,阴极的反应式为2 MnO42--2e-═2 MnO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
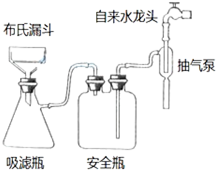 某学生预测定味精(味精的主要成分化学式为C5H8NO4Na•H2O)中食盐的含量,做了如下实验:
某学生预测定味精(味精的主要成分化学式为C5H8NO4Na•H2O)中食盐的含量,做了如下实验: .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com