
| A、10mL H2O |
| B、0.1mol HCl |
| C、24g Mg |
| D、1g CaCO3 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
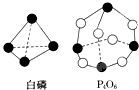 化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:E(P-P)=198kJ?mol-1、E(P-O)=360kJ?mol-1、E(O=O)=498kJ?mol-1,则反应P4(白磷)燃烧生成P4O6的热化学方程式为
化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:E(P-P)=198kJ?mol-1、E(P-O)=360kJ?mol-1、E(O=O)=498kJ?mol-1,则反应P4(白磷)燃烧生成P4O6的热化学方程式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、11.2L氧气所含的原子数为NA |
| B、1.9g的H3O+离子中含有的电子数为11NA |
| C、常温常压下96g NO2与N2O4的混合物含有的氧原子数为2NA |
| D、0.5mol/LH2SO4中的H+数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、需要加热才能发生的反应一定是吸热反应 |
| B、任何放热反应在常温条件下一定能够发生 |
| C、反应物和生成物所具有的总能量的差决定了化学反应是放热还是吸热 |
| D、构成物质微粒间的化学键键能越小,该物质的能量就越低,物质越稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(1)(2)(6) |
| B、(1)(2)(4)(6) |
| C、(2)(6) |
| D、(2)(4)(6) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 探究内容 | 实验方案 | 实验现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com