
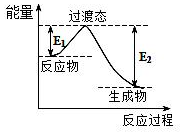
| A£® |  ÓÉČēĶ¼ÖŖ£¬ŹÆÄ«×Ŗ±äĪŖ½šøÕŹÆŹĒ·ÅČČ·“Ó¦ | |
| B£® |  ÓÉČēĶ¼ÖŖ£¬S£Øg£©+O2£Øg£©ØTSO2£Øg£©”÷H1£¬S£Øs£©+O2£Øg£©ØTSO2£Øg£©”÷H2Ōņ”÷H1£¼”÷H2 | |
| C£® |  ÓÉČēĶ¼ÖŖ£¬°×Į×±ČŗģĮ×ĪČ¶Ø | |
| D£® |  ČēÓÉĶ¼ÖŖ£¬CO£Øg£©+H2O£Øg£©ØTCO2£Øg£©+H2£Øg£©”÷H£¾0 |
·ÖĪö A£®øł¾ŻĶ¼ĻóÅŠ¶ĻÄÜĮæøßµĶ£¬ŅŌ“ĖÅŠ¶Ļ·“Ó¦ČČ£»
B£®ČēÉś³ÉĪļĻąĶ¬£¬Ōņ·“Ó¦Īļ×ÜÄÜĮæŌ½“󣬷ÅČČŌ½¶ą£¬×¢Ņā·“Ó¦ČČĪŖøŗÖµ£»
C£®ÄÜĮæŌ½øßŌ½²»ĪČ¶Ø£»
D£®ÓÉĶ¼ĻóæÉÖŖCO£Øg£©+H2O£Øg£©×ÜÄÜĮæCO2£Øg£©+H2£Øg£©“óÓŚ×ÜÄÜĮ森
½ā“š ½ā£ŗA£®ÓÉĶ¼ĻóæÉÖŖ½šøÕŹÆµÄÄÜĮæ±ČŹÆÄ«µÄÄÜĮæøߣ¬ŌņÄ«×Ŗ±äĪŖ½šøÕŹÆŹĒĪüČČ·“Ó¦£¬¹ŹA“ķĪó£»
B£®ĻąĶ¬Ģõ¼žĻĀ£¬µČÖŹĮæS£Øg£©ŗĶS£Øs£©µÄÄÜĮæ±Č½Ļ£¬S£Øs£©½ĻŠ”£¬ŌņĻąĶ¬ĪļÖŹµÄĮæµÄS£Øg£©±ČS£Øs£©ĶźČ«·“Ó¦Ź±·ÅČȶą£¬ŅņĪŖ·ÅČČ·“Ó¦£¬”÷H£¼0£¬Ōņ”÷H1£¼”÷H2£¬¹ŹBÕżČ·£»
C£®ÓÉĶ¼ĻóæÉÖŖ°×Į×±ČŗģĮ×ÄÜĮæøߣ¬Ōņ°×Į×½Ģ²»ĪČ¶Ø£¬¹ŹC“ķĪó£»
D£®ÓÉĶ¼ĻóæÉÖŖCO£Øg£©+H2O£Øg£©×ÜÄÜĮæCO2£Øg£©+H2£Øg£©“óÓŚ×ÜÄÜĮ棬ŌņCO£Øg£©+H2O£Øg£©ØTCO2£Øg£©+H2£Øg£©ĪŖ·ÅČČ·“Ó¦£¬”÷H£¼0£¬¹ŹD“ķĪó£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ·“Ó¦ÓėÄÜĮæ±ä»Æ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬עŅā°ŃĪÕĶ¼ĻóµÄĢŲµć£¬ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£¬“šĢāŹ±×¢ŅāÉóĢā£¬ÄŃ¶Č²»“ó£®


 ĘŚÄ©³å“Ģ100·Ö““ŠĀ½š¾ķĶźČ«ŹŌ¾ķĻµĮŠ“š°ø
ĘŚÄ©³å“Ģ100·Ö““ŠĀ½š¾ķĶźČ«ŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ĪĀ¶Č/”ę | 700 | 830 | 1200 |
| KÖµ | 1.7 | 1.0 | 0.4 |
| A£® | 4sŹ±£¬c£ØB£©ĪŖ0.76 mol•L-1 | |
| B£® | 830”ęµ½Ę½ŗāŹ±£¬AµÄ×Ŗ»ÆĀŹĪŖ80% | |
| C£® | “ļĘ½ŗāŹ±£¬ÉżøßĪĀ¶Č£¬Ę½ŗāÕżĻņŅĘ¶Æ | |
| D£® | 1200”ꏱ·“Ó¦C£Øg£©+D£Øg£©?A£Øg£©+B£Øg£©µÄĘ½ŗā³£ŹżµÄÖµĪŖ0.4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉżøßĪĀ¶Č£¬W µÄĢå»ż·ÖŹż¼õŠ”£¬”÷H Ōö“ó | |
| B£® | ŅŌ Y µÄÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ 0.01 mol/£ØL•s£© | |
| C£® | ŌŚĘäĖüĢõ¼ž²»±äµÄĒéæöĻĀ£¬Ōö¼Ó 1 mol X£¬Ōņ X ŗĶ Y µÄ×Ŗ»ÆĀŹ¾łĢįøß | |
| D£® | ŌŁĻņČŻĘ÷ÖŠĶØČė 2 mol X ŗĶ 1 mol Y£¬“ļµ½Ę½ŗāŹ±£¬X”¢Y µÄ×Ŗ»ÆĀŹ¾łŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
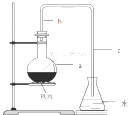 ֊ѧŹµŃéŹŅÓĆČēĶ¼ĖłŹ¾×°ÖĆÖĘȔɣĮæäå±½£®ĒėĢīŠ“ĻĀĮŠæÕ°×£®
֊ѧŹµŃéŹŅÓĆČēĶ¼ĖłŹ¾×°ÖĆÖĘȔɣĮæäå±½£®ĒėĢīŠ“ĻĀĮŠæÕ°×£®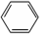 +Br2$\stackrel{FeBr_{3}}{”ś}$
+Br2$\stackrel{FeBr_{3}}{”ś}$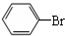 +HBr£®
+HBr£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
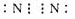 £®
£®| B-A | B-D | B=D | A-A | A-D |
| 413.4 | 351 | 745 | 436 | 462.8 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com