
| A. | 2:1:2 | B. | 1:2:1 | C. | 1:1:1 | D. | 2:2:1 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
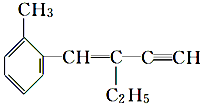
| A. | 该有机物结构简式为C13H14 | |
| B. | 该有机物属于苯的同系物 | |
| C. | 该有机物分子中至少有6个碳原子共平面 | |
| D. | 该有机物能与溴水发生加成反应且1mol该有机物最多能加成3mol的Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃烧煤炭供热会加剧“温室效应“ | |
| B. | 将废旧电池深埋处理,可有效防止电池中的重金属污染 | |
| C. | 预防H7N9流感病毒的措施之一是高温消毒餐具等生活日用品 | |
| D. | 开发利用太阳能、风能、生物能、海洋能等清洁能源,符合“低碳经济” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用FeCl3溶液可鉴别化合物A和分支酸 | |
| B. | 化合物A中含有3个手性碳原子 | |
| C. | 1mol分支酸在一定条件下最多可与2molNaHCO3发生反应 | |
| D. | 在浓硫酸和加热条件下,化合物A可发生消去反应生成多种有机产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2 +H2SO4 ═BaSO4↓+2H2O | B. | BaCO3 +2HNO3═Ba(NO3)2 +CO2↑+H2O | ||
| C. | NaOH+HCl═NaCl+H2O | D. | Mg(OH)2 +2HCl═Mg Cl2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com