
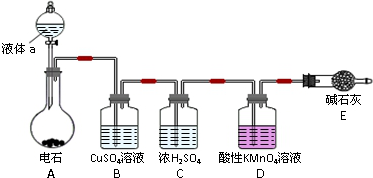
分析 (1)实验室制取乙炔时,用饱和食盐水与电石反应制得;
(2)因为电石里含有许多杂质,所以用饱和食盐水与电石反应制乙炔,会引入H2S、PH3、AsH3等杂质;
根据方程式由高锰酸钾的物质的量求出乙炔的物质的量,再根据装置D及E的总质量共增重y g,即乙炔质量为yg,可求出乙炔的相对分子质量.
解答 解:(1)实验室制取乙炔时,用饱和食盐水与电石反应制得,所以分液漏斗中的液体a通常是饱和食盐水,故答案为:饱和食盐水;
(2)因为电石里含有许多杂质,所以用饱和食盐水与电石反应制乙炔,会引入H2S、PH3、AsH3等杂质,所以B中的CuSO4用于除去乙炔中混有的H2S、PH3、AsH3等杂质,故答案为:除去乙炔中混有的H2S、PH3、AsH3等杂质;
(3)根据原子守恒,所以乙炔与酸性KMnO4溶液反应方程式为:C2H2+2KMnO4+3H2SO4═K2SO4+2MnSO4+2CO2↑+4H2O,又D中过量的KMnO4恰好能与含z mol FeSO4的溶液完全反应,反应方程式为10FeSO4+2KMnO4+8H2SO4═K2SO4+5Fe2(SO4)3+2MnSO4+8H2O,则n(C2H2)=$\frac{1}{2}$n(KMnO4)=$\frac{1}{2}$(x-$\frac{z}{5}$)mol,乙炔的质量等于装置D及E的总质量共增重的质量,故m(C2H2)=yg,所以M=$\frac{m}{n}$=$\frac{10y}{5x-z}$g/mol,即相对分子质量为$\frac{10y}{5x-z}$,故答案为:$\frac{10y}{5x-z}$.
点评 本题考查了测定乙炔相对分子质量的方法,乙炔的制备,除杂,影响因素等,比较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
| 化学键 | H-H | C-O |  | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1076 | 465 | 413 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应时间/min | n(CO)/mol | n(H2O)/mol | n(CO2)/mol | n(H2)/mol |
| 0 | 1.20 | 0.60 | 0 | 0 |
| t1 | 0.80 | |||
| t2 | 0.20 |
| A. | 反应在t1min末的速率为v(H2)=0.2/t mol•L-1•min-1 | |
| B. | 平衡时水蒸气的转化率为66.67% | |
| C. | 该温度下反应的平衡常数为l | |
| D. | 其他条件不变,若起始时,n(CO)=0.60 mol,n(H2O)=1.20 mol,则平衡时水蒸气的转化率为33.33% |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | K1=$\frac{[{H}_{2}]^{4}}{[{H}_{2}O]^{4}}$ | |
| B. | 增大c(H2O)或减小c(H2),会使平衡常数K1减小 | |
| C. | 改变反应的温度,平衡常数K1不一定变化 | |
| D. | Fe3O4(s)+4H2(g)?3Fe(s)+4H2O(g)的平衡常数为K2,K1×K2=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雾屑于胶体,能产生丁达尔现象 | |
| B. | 大雾的形成与汽车的尾气排放没有关系 | |
| C. | 持续大雾天气给农业生产、交通运输等带来很大的影响 | |
| D. | 空气中悬浮的细小颗粒物严重危害人体健康 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
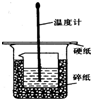 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{200a}{m}$mol-1 | B. | $\frac{200m}{a}$mol-1 | C. | $\frac{2m}{a}$mol-1 | D. | $\frac{2a}{m}$mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
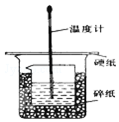 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:| 实验序号 | 起始温州 t1/℃ | 终止温度(t2)/℃[ | 温差 (t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下,测得某HA溶液中c(HA)=0.01mol•L-1 | |
| B. | 碳酸钠溶液中滴入0.1mol•L-1的HA溶液,产生大量无色气体 | |
| C. | 室温下测得某HA溶液的pH=a,用蒸馏水稀释100倍测得溶液pH=b,且b-a<2 | |
| D. | 室温下,测得0.1mol•L-1HA溶液的pH>1,证明HA是弱酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com