
·ÖĪö £Ø1£©·“Ó¦ŗóµĆµ½MClČÜŅŗ£¬²āµĆ»ģŗĻČÜŅŗµÄpH=6£¬Ė®½ā³ŹĖįŠŌ£¬ŌņÓɵēŗÉŹŲŗćæÉÖŖc£ØH+£©+c£ØM+£©=c£ØCl-£©+c£ØOH-£©£»
£Ø2£©0.5mol/LµÄHClČÜŅŗŗĶ°±Ė®»ģŗĻŗóČÜŅŗĒ”ŗĆ³ŹÖŠŠŌ£¬ČōĢå»żĻąĶ¬£¬Éś³ÉĀČ»Æļ§ĻŌĖįŠŌ£»
£Ø3£©pH=3µÄHRČÜŅŗÓėpH=11µÄNaOHČÜŅŗµČĢå»ż»ģŗĻ£¬²āµĆ»ģŗĻČÜŅŗµÄpH”Ł7£¬ŌņHRĪŖČõĖį£»
£Ø4£©Ė®½āÉś³ÉµÄHClŅ×»Ó·¢£»
£Ø5£©ļ§øłĄė×ÓĖ®½āĻŌĖįŠŌ£®
½ā“š ½ā£ŗ£Ø1£©·“Ó¦ŗóµĆµ½MClČÜŅŗ£¬²āµĆ»ģŗĻČÜŅŗµÄpH=6£¬Ė®½ā³ŹĖįŠŌ£¬ŌņÓɵēŗÉŹŲŗćæÉÖŖc£ØH+£©+c£ØM+£©=c£ØCl-£©+c£ØOH-£©£¬Ōņc£ØCl-£©-c£ØM+£©=10-6mol/L-10-8mol•L-1=9.9”Į10-7mol/L£¬¹Ź“š°øĪŖ£ŗ9.9”Į10-7£»
£Ø2£©0.5mol/LµÄHClČÜŅŗŗĶ°±Ė®»ģŗĻŗóČÜŅŗĒ”ŗĆ³ŹÖŠŠŌ£¬ČōĢå»żĻąĶ¬£¬Éś³ÉĀČ»Æļ§ĻŌĖįŠŌ£¬ĪŖ±£Ö¤ĻŌÖŠŠŌ£¬¼ī¹żĮ棬Ōņ»ģŗĻĒ°HClČÜŅŗµÄĢå»żŠ”ÓŚ°±Ė®µÄĢå»ż£¬
¹Ź“š°øĪŖ£ŗŠ”ÓŚ£»
£Ø3£©pH=3µÄHRČÜŅŗÓėpH=11µÄNaOHČÜŅŗµČĢå»ż»ģŗĻ£¬²āµĆ»ģŗĻČÜŅŗµÄpH”Ł7£¬ŌņHRĪŖČõĖį£¬·“Ӧɜ³ÉĒæ¼īČõĖįŃĪ£¬ĒŅĖį¹żĮ棬ČÜŅŗĻŌĖįŠŌ£¬pH£¼7£¬
¹Ź“š°øĪŖ£ŗ£¼7£»
£Ø4£©°ŃFeCl3ČÜŅŗÕōøÉ”¢×ĘÉÕ£¬Ė®½āÉś³ÉµÄHCl»Ó·¢£¬µĆµ½ĒāŃõ»ÆĢś×ĘČČ·Ö½āÉś³ÉŃõ»ÆĢś£¬Ōņ×īŗóµĆµ½µÄ¹ĢĢå²śĪļÖ÷ŅŖŹĒFe2O3£¬¹Ź“š°øĪŖ£ŗFe2O3£»
£Ø5£©NH4ClČÜŅŗ³ŹĖįŠŌµÄŌŅņĪŖNH4++H2O?NH3•H2O+H+£¬¹Ź“š°øĪŖ£ŗNH4++H2O?NH3•H2O+H+£®
µćĘĄ ±¾Ģāæ¼²éĖį¼ī»ģŗĻµÄ¶ØŠŌÅŠ¶ĻŗĶ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦µÄ漲飬øł¾ŻµēŗÉŹŲŗćŗĶÖŹ×ÓŹŲŗć·ÖĪöČõµē½āÖŹµÄµēĄė¼°ŃĪĄąĖ®½ā£¬ĢāÄæÄŃ¶Č²»“ó£®


 A¼Ó½šĢā ĻµĮŠ“š°ø
A¼Ó½šĢā ĻµĮŠ“š°ø Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø
Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| »ÆŗĻĪļ | Mg£ØOH£©2 | Al£ØOH£©3 | Cr£ØOH£©3 |
| ĶźČ«³ĮµķµÄPh | 10.5 | 4.3 | 5.3 |
| æŖŹ¼ČܽāµÄpH | -- | 7.8 | 9.2 |
| Ksp½üĖĘÖµ | 10-12 | 10-14 | 10-31 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 299 | B£® | 598 | C£® | 587 | D£® | 447 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
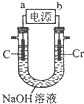
 ČēĶ¼ĖłŹ¾£¬¼×”¢ŅŅĮ½³ŲµÄµē¼«²ÄĮĻ¶¼ŹĒĢś°ōÓėĢ¼°ō£¬±ū³ŲŹĒµē½ā¾«Į¶Ķ£®
ČēĶ¼ĖłŹ¾£¬¼×”¢ŅŅĮ½³ŲµÄµē¼«²ÄĮĻ¶¼ŹĒĢś°ōÓėĢ¼°ō£¬±ū³ŲŹĒµē½ā¾«Į¶Ķ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ·“Ó¦¢ŁĖµĆ÷SO2¾ßÓŠĘư׊Ō£¬·“Ó¦¢ŚĖµĆ÷SO2¾ßÓŠĖįŠŌ | |
| B£® | ·“Ó¦¢ŚÖŠÉś³ÉĪļn£ØNa2SO3£©£ŗn£ØNaHSO3£©=1£ŗ1Ź±£¬Ōņ·“Ó¦Īļn£ØSO2£©£ŗn£ØNaOH£©=1£ŗ2 | |
| C£® | ·“Ó¦¢Ū¢Ü¢Ż¾łŹōÓŚŃõ»Æ»¹Ō·“Ó¦ | |
| D£® | ¹¤ŅµÉĻæÉĄūÓĆ·“Ó¦¢ŚŗĶ·“Ó¦¢Ü»ŲŹÕSO2 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com