
| A. | ① | B. | ② | C. | ③ | D. | ④ |
分析 水中H元素的化合价降低,则水为氧化剂,若水中O元素的化合价升高,则水为还原剂,以此来解答.
解答 解:①Cl2+H2O=HCl+HClO中,水中H、O元素的化合价不变,Cl元素的化合价由0价变为+1价和-1价,所以该反应是氧化还原反应,但水既不是氧化剂又不是还原剂;
②3NO2+H2O=2HNO3+NO中,N元素的化合价由+4价变为+5价和+2价,水中H、O元素的化合价不变,所以该反应是氧化还原反应,但水既不是氧化剂又不是还原剂;
③2Na+2H2O=2NaOH+H2↑中,水中H元素的化合价降低,则水为氧化剂;
④2Na2O2+2H2O=4NaOH+O2↑中,过氧化钠中氧元素的化合价由-1价变为0价和-2价,水中H、O元素的化合价不变,所以该反应是氧化还原反应,但水既不是氧化剂又不是还原剂;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意水中H、O元素的化合价分析,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | SiCl4 | SiHCl3 | AlCl3 | FeCl3 |
| 沸点/℃ | 57.7 | 33.0 | - | 315 |
| 升华温度/℃ | - | - | 180 | 300 |
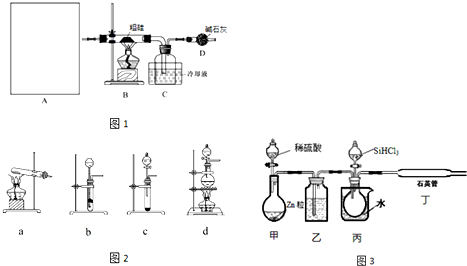
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据元素组成可判断是化合物 | |
| B. | 因它电离会生成钠离子又符合盐的组成,故可属于钠盐 | |
| C. | 因它电离会生成硫酸根离子又符合盐的组成,故可属于硫酸盐 | |
| D. | NaHSO4溶于水可电离出氢离子故可以称为酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ/mol.
(1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 25 | t1 | t2 |
| Kw/mol2•L-2 | 1×10-14 | a | 1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B的阳离子的氧化性比A的阳离子强,说明A元素的金属性一定比B元素强 | |
| B. | 发生氧化还原反应时,A原子失去的电子比B原子多,证明A的金属性一定比B强 | |
| C. | 适量的Cl2通入FeI2溶液中可发生反应:3Cl2+6FeI2=2FeCl3+4FeI3 | |
| D. | 一定量氯气通入30 mL 10.00 mol•L-1的氢氧化钠溶液中,加热后形成NaCl、NaClO、NaClO3共存的溶液,若反应中转移的电子为n mol,则0.15<n<0.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖和维生素C中含有的碳、氧原子个数相等 | |
| B. | 葡萄糖和维生素C中碳元素和氧元素的质量比都是l:1 | |
| C. | -个葡萄糖分子比-个维生素C分子多4个氢原子 | |
| D. | -个维生素C分子中的中子数和电子数一定相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com