
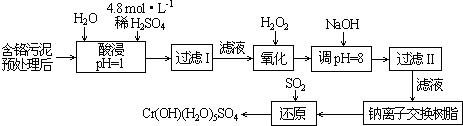
| ������ | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| ��ʼ����ʱ��pH | 1.9 | 7.0 | -- | -- | 4.7 | -- |
| ������ȫʱ��pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9 ����9�ܽ⣩ |


 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
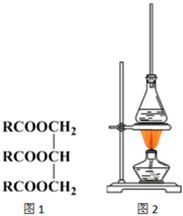 ��֬�Ǹ�֬����ĸ���������ṹ���Ա�ʾΪͼ1��RΪ��ͬ���ţ���������֬��������Ӧ�͵ζ������Բⶨ��֬��ƽ�����������ش��������⣺
��֬�Ǹ�֬����ĸ���������ṹ���Ա�ʾΪͼ1��RΪ��ͬ���ţ���������֬��������Ӧ�͵ζ������Բⶨ��֬��ƽ�����������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
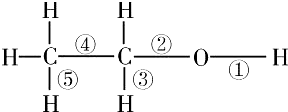
| A������ᡢŨ���Ṳ��ʱ���Ѣ� |
| B���ڿ�����ȼ��ʱ���Ѣܢ� |
| C���ͽ����Ʒ�Ӧʱ���Ѣ� |
| D����Cu���º�O2��Ӧʱ���Ѣڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������Һ�еμ������BaCl2��Һ��������ɫ��������˵�������к���SO42- |
| B��������Һ�еμ������BaCl2��Һ��������������˵�������в���SO42- |
| C��������ˮ�еμ�ϡHNO3��AgNO3��Һ��������ɫ��������˵������ˮ�к���Cl- |
| D��������ˮ�еμ�ϡHNO3��AgNO3��Һ��������ɫ��������˵������ˮ�к���Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| O2 |
| �� |
| O2 |
| �� |
| H2O |
| �� |
| A����XΪN2��NH3����AΪ���� |
| B����XΪS��H2S����AΪ���� |
| C����XΪ�ǽ������ʻ�ǽ����⻯���A��һ���������ͭ��Ӧ����Y |
| D����Ӧ�ٺ�һ��Ϊ������ԭ��Ӧ����Ӧһ��Ϊ��������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ӧ��HA��Һ������ʣ�� |
| B��������NaA��ˮ��Һ��pH����С��7 |
| C��HA��Һ��NaOH��Һ��������ܲ���� |
| D��HA��Һ��c��H+����NaOH��Һ��c��OH-�� ���ܲ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com