
分析 ①A与B反应有气体生成,则A、B分别为HCl、NaHSO4、Na2CO3中的一种;
②B与C反应有沉淀生成,则沉淀可能为硫酸钡、也可能为AgCl;
③C与D反应有沉淀生成,结合在②和③的反应中生成的沉淀是同一种物质,沉淀应为AgCl,则C为AgNO3,B为HCl,D为BaCl2;
⑤A与E反应有气体生成、④D与E反应有沉淀生成,则A为Na2CO3,E为NaHSO4,以此来解答.
解答 解:①A与B反应有气体生成,则A、B分别为HCl、NaHSO4、Na2CO3中的一种;
②B与C反应有沉淀生成,则沉淀可能为硫酸钡、也可能为AgCl;
③C与D反应有沉淀生成,结合在②和③的反应中生成的沉淀是同一种物质,沉淀应为AgCl,则C为AgNO3,B为HCl,D为BaCl2;
⑤A与E反应有气体生成、④D与E反应有沉淀生成,则A为Na2CO3,E为NaHSO4,
由上述分析可知,B、C、D分别为HCl、AgNO3、BaCl2;
(1)③的反应中,生成的沉淀物质为AgCl;故答案为:AgCl;
(2)C为AgNO3,B为HCl,D为BaCl2;故答案为:HCl、AgNO3、BaCl2;
(3)A与E反应的离子方程式是2H++CO32-=H2O+CO2↑,故答案为:CO32-+2H+=CO2↑+H2O.
点评 本题考查物质的鉴别,为高频考点,把握物质的性质及反应中的现象为鉴别推断物质的关键,注意物质之间的相互反应,推断②③中沉淀为AgCl为解答的突破口,题目难度中等.


科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ | ||||
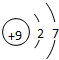 ;最高价氧化物对应的水化物中碱性最强的是NaOH(填化学式)
;最高价氧化物对应的水化物中碱性最强的是NaOH(填化学式)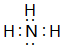 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热反应中反应物的总焓大于生成物的总焓 | |
| B. | 原子组成分子一定放出热量 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 化石燃料在地球上的蕴藏量是有限的,而且又都是经过亿万年才能形成的非再生资源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量金属钠保存在煤油中 | |
| B. | 试剂瓶中的液溴可用水封存,防止溴挥发 | |
| C. | 保存硫酸亚铁溶液时,要向其中加入少量硫酸和铁粉 | |
| D. | 浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
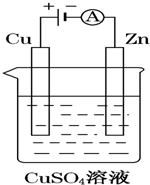 如图是一个电解过程示意图.
如图是一个电解过程示意图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{\;}^{13}$O和14O互称同素异形体 | B. | 丙烷和异丁烷互称同系物 | ||
| C. | 金刚石和石墨互称同位素 | D. | 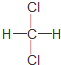 和 和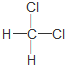 互称同分异构体 互称同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com