
分析 氯气溶于水发生反应Cl2+H2O?HCl+HClO,根据方程式知,溶液中的成分是氯气、水、盐酸和次氯酸,其中次氯酸具有漂白性,结合酸性、漂白性、氧化性来解答,
(1)氯水中含有的微粒有分子Cl2、H2O、HClO,离子为H+、ClO-、OH-、Cl-;
(2)氯气为黄绿色气体,氯气溶于水中的氯气分子为黄绿色;
(3)将氯水滴在石灰石上有气泡产生,是利用氯水中的氢离子和碳酸钙反应生成二氧化碳气体;
(4)氯离子与银离子结合生成沉淀;
(5)氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性.
解答 解:氯气溶于水发生反应Cl2+H2O?HCl+HClO,根据方程式知,溶液中的成分是氯气、水、盐酸和次氯酸,
(1)氯水中含有的微粒有分子Cl2、H2O、HClO,离子为H+、ClO-、OH-、Cl-,
故答案为:Cl2、H2O、HClO、H+、ClO-、OH-、Cl-;
(2)氯气为黄绿色气体,使氯水呈现黄绿色的是Cl2,故答案为:Cl2;
(3)将氯水滴在石灰石上有气泡产生,是利用氯水中的氢离子和碳酸钙反应生成二氧化碳气体,反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:H+;CaCO3+2H+=Ca2++CO2↑+H2O;
(4)氯离子与银离子结合生成沉淀,能使硝酸银溶液产生白色沉淀的是Cl-(HCl),反应的离子方程式是为:Ag++Cl-=AgCl↓,
故答案为:Cl-(HCl);Ag++Cl-=AgCl↓;
(5)氯气和水反应生成盐酸和次氯酸,其中HClO具有漂白性,能使湿润的有色布条褪色的是HClO,故答案为:HClO.
点评 本题考查氯气的性质,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,为高频考点,注意氯水的成分及性质,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不是所有的烷烃中都既有极性键,又有非极性键 | |
| B. | 所有的烯烃中都是既有极性键,又有非极性键 | |
| C. | 在CCl4中碳元素呈现+4价 | |
| D. | 有机化学反应只能发生在极性键上 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KOH | B. | KAl(SO4)2 | C. | KHCO3 | D. | K2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
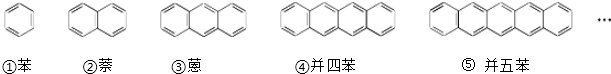
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极得电子反应产物是Mn2O3(s) | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 外电路中每通过O.2mol电子,锌的质量理论上减小6.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
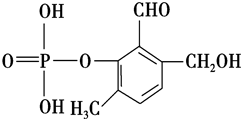
| A. | 能与金属钠反应 | |
| B. | 能使石蕊试液变红 | |
| C. | 能发生银镜反应 | |
| D. | 1mol该酯与NaOH溶液反应,最多消耗3molNaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com