
| ���� |
| �� |
| ���� |
| �� |
| ���� |
| �� |
| ���� |
| �� |
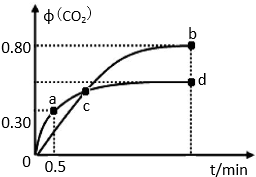
| n��SO32-����n��HSO3-�� | 91��9 | 1��1 | 9��91 |
| c��H+�� | 6.3��10-9 | 6.3��10-8 | 6.3��10-7 |
| c(SO32-)��c(H+) |
| c(HSO3-) |
| x |
| 4 |
| 1.2mol |
| 2L��0.5min |
| y |
| 4 |
| c(CO2)5 |
| c(CO)5 |
| 1��65 |
| 0��45 |
| c(SO32-)��c(H+) |
| c(HSO3-) |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 COOH
COOH�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ۢ� | B���٢ܢ� |
| C���ڢ� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
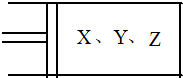 ��ͼ��ʾ����6mol X��3mol Y���������������ɱ�ĵ�ѹ�����У���һ���¶��·������·�Ӧ��2X��g��+Y��g��?2Z��g������Ӧ�ﵽƽ��״̬Aʱ��������������ʵ���Ϊ6.6mol����X��Y��Z����ʼ���ʵ����ֱ���a��b��c��ʾ���ش��������⣺
��ͼ��ʾ����6mol X��3mol Y���������������ɱ�ĵ�ѹ�����У���һ���¶��·������·�Ӧ��2X��g��+Y��g��?2Z��g������Ӧ�ﵽƽ��״̬Aʱ��������������ʵ���Ϊ6.6mol����X��Y��Z����ʼ���ʵ����ֱ���a��b��c��ʾ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��AgCl������ˮ����Һ��û��Ag+��Cl- |
| B��AgCl�������ɺ��ܽ�ͬʱ�ڲ��Ͻ��У���������� |
| C����AgCl��Һ�м������ᣬһ�����г������� |
| D������AgCl������Һ�м���NaBr���壬AgCl�������仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
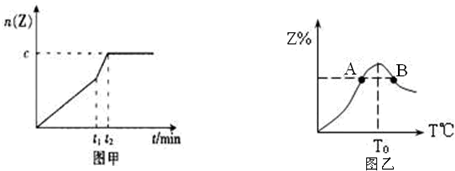
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��78g Na2O2������CO2��ַ�Ӧʱ����ת����Ϊ2NA |
| B��NA���������ӵ����Ϊ22.4L |
| C��4�桢101kPaʱ��54mL H2O�к��еķ�����Ϊ3NA |
| D��1mol/L Na2SO4��Һ����������Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������������ֺͻ�ͭ�����ںϽ� |
| B��ˮ�ࡢ�������մɾ��������ǽ������� |
| C�������ơ�����þ�������������ڼ��������� |
| D����Һ�����塢��Һ�����ڷ�ɢϵ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com