
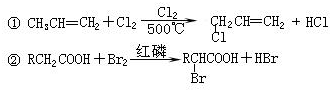
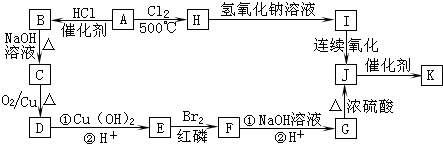
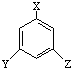
 ,又能发生银镜反应,遇FeCl3溶液又能呈紫色的同分异构体有
,又能发生银镜反应,遇FeCl3溶液又能呈紫色的同分异构体有| 118 |
| 12 |
| 2×9+2-10 |
| 2 |
 ,与氯气在加热条件下发生取代反应生成H为
,与氯气在加热条件下发生取代反应生成H为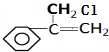 ,则I为
,则I为 ,J为
,J为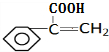 .结合C能发生催化氧化,则A与HCl发生加成反应生成B为
.结合C能发生催化氧化,则A与HCl发生加成反应生成B为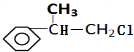 ,顺推可知C为
,顺推可知C为 ,D为
,D为 ,E为
,E为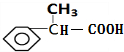 ,结合反应信息可知F为
,结合反应信息可知F为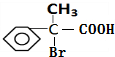 ,则G为
,则G为 ,G发生消去反应生成J,J发生加聚反应生成K为
,G发生消去反应生成J,J发生加聚反应生成K为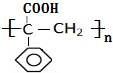 ,据此解答.
,据此解答.| 118 |
| 12 |
| 2×9+2-10 |
| 2 |
 ,与氯气在加热条件下发生取代反应生成H为
,与氯气在加热条件下发生取代反应生成H为 ,则I为
,则I为 ,J为
,J为 .结合C能发生催化氧化,则A与HCl发生加成反应生成B为
.结合C能发生催化氧化,则A与HCl发生加成反应生成B为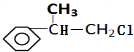 ,顺推可知C为
,顺推可知C为 ,D为
,D为 ,E为
,E为 ,结合反应信息可知F为
,结合反应信息可知F为 ,则G为
,则G为 ,G发生消去反应生成J,J发生加聚反应生成K为
,G发生消去反应生成J,J发生加聚反应生成K为 ,
, ,C为
,C为 ,含有的官能团的名称为:羟基,故答案为:
,含有的官能团的名称为:羟基,故答案为: ;羟基;
;羟基; )通过酯化反应形成环酯或3分子之间发生酯化反应形成链状酯,可制得含三个六元环的有机物的结构简式为:
)通过酯化反应形成环酯或3分子之间发生酯化反应形成链状酯,可制得含三个六元环的有机物的结构简式为: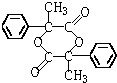 或
或 ,
, 或
或 ;
; ,
,
| 催化剂 |
 ,
, ;n
;n
| 催化剂 |
 ;
; )的同分异构体有多种,则其中属于苯的三取代物,满足结构为
)的同分异构体有多种,则其中属于苯的三取代物,满足结构为 ,又能发生银镜反应,遇FeCl3溶液又能呈紫色,含有酚羟基、-CHO,故侧链为-OH、-CHO、-CH2CH3,或侧链为-OH、-CH2CHO、-CH3,符合条件的同分异构体有2种,故答案为:2.
,又能发生银镜反应,遇FeCl3溶液又能呈紫色,含有酚羟基、-CHO,故侧链为-OH、-CHO、-CH2CH3,或侧链为-OH、-CH2CHO、-CH3,符合条件的同分异构体有2种,故答案为:2.


科目:高中化学 来源: 题型:
| A、② | B、①③⑥ | C、②④ | D、①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
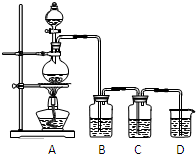 已知单质硫是淡黄色粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
已知单质硫是淡黄色粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 操作 | 现象 |
| Ⅰ |  | 反应剧烈,试管中的黑色固体逐渐溶解,产生大量的无色具有臭鸡蛋气味的气体. |
| Ⅱ | 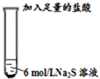 | 只有少量的无色臭鸡蛋气味的气体产生,但溶液中却有一定量的淡黄色沉淀产生. |
| 编号 | 操作 | 现象 |
| Ⅲ | 将H2S通入蒸馏水中达到饱和,将该溶液分为两等份.一份静置,另一份在空气中不断振荡. | 两份溶液在短时间内均未出现明显的浑浊现象. |
| 编号 | 操作 | 现象 |
| Ⅳ | 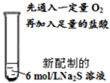 | 先通入一定量O2,几乎看不到明显变化;加入足量的盐酸,产生无色具有臭鸡蛋气味的气体,溶液中有大量的淡黄色沉淀产生. |
查看答案和解析>>
科目:高中化学 来源: 题型:
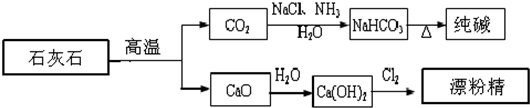
| A、漂粉精是混合物,主要成分是氯化钙 |
| B、图示的制纯碱方法,要求先向饱和食盐水中通NH3,然后再通CO2 |
| C、纯碱属于碱,俗名苏打 |
| D、制取纯碱和漂粉精所涉及的反应都是非氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
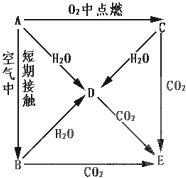 A、B、C、D、E五种物质都含有同一种活泼金属元素,它们按图所示关系相互转化,已知A为单质.
A、B、C、D、E五种物质都含有同一种活泼金属元素,它们按图所示关系相互转化,已知A为单质.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、T℃时,饱和CaCO3溶液与饱和CaF2溶液相比,后者Ca2+浓度大 |
| B、T℃时,饱和CaCO3溶液与饱和CaF2溶液等体积混合,会析出CaCO3固体 |
| C、T℃时,CaF2固体在20mL0.01 mol?L-1盐酸中的Ksp比在纯水中的Ksp大 |
| D、T℃时,在CaCO3悬浊液中加入NaF固体,CaCO3不可能转化为CaF2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com