
| A. | 蛋白质“溶液”是一种胶体,向该分散系中加入少量的盐(如硫酸铵)能促进蛋白质的溶解 | |
| B. | 饱和(NH4)2SO4溶液能使蛋白质变性 | |
| C. | 用半透膜可除去蛋白质溶液中的NaCl | |
| D. | 用灼烧的方法检验是毛线还是棉线 |
分析 A.B.饱和硫酸铵溶液可使蛋白质的溶解性变小,此过程叫做蛋白质的“盐析”;
C.胶粒不能透过半透膜;
D.毛线的成分为蛋白质,灼烧有烧焦羽毛的气味.
解答 解:A.向蛋白质“溶液”中加入饱和硫酸铵溶液,可以观察到的现象为析出沉淀,故A正确;
B.饱和(NH4)2SO4溶液能使蛋白质发生盐析,不发生变性,故B错误;
C.蛋白质溶液是胶体,胶粒不能透过半透膜,可用渗析提纯胶体,故C正确;
D.毛线的成分为蛋白质,灼烧有烧焦羽毛的气味,则用灼烧的方法检验是毛线还是棉线,故D正确.
故选B.
点评 本题考查化学实验方案评价,为高频考点,侧重考查物质鉴别、物质检验等知识点,明确物质性质及实验原理即可解答,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
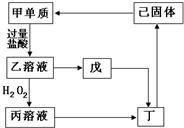 已知甲、乙、丙、丁、戊、己六种物质中含同一种元素,它们之间的转化关系如图所示.其中,丁是一种红褐色沉淀,戊是一种白色沉淀.请回答下列问题:
已知甲、乙、丙、丁、戊、己六种物质中含同一种元素,它们之间的转化关系如图所示.其中,丁是一种红褐色沉淀,戊是一种白色沉淀.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ClO3-,Cl-,K+ | B. | ClO-,Cl-,H+ | ||
| C. | NaClO,NaClO3,NaNO3 | D. | NaClO,Na2SO4,NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含0.1 mol Na+、0.2 mol Mg2+、0.1 mol Cl-和0.1 mol NO3-的溶液 | |
| B. | 只含0.1 mol NH4+、0.1 mol Ca2+、0.1 mol CO32-和0.1 mol Cl-的溶液 | |
| C. | 为了通过测定pH的大小,达到比较HCl和CH3COOH酸性强弱的目的,分别配制100 mL 0.1 mol/L的NaCl溶液和CH3COONa溶液 | |
| D. | 仅用1 000 mL的容量瓶、烧杯、玻璃棒、量筒、58.5 g NaCl固体和水配制1 L 1 mol/L的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑧⑨ | B. | ⑤⑦⑧⑨⑩ | C. | ②③④⑤⑦ | D. | ①⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com