
| A£® | 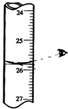 ¶ĮČ”µĪ¶Ø | B£® | 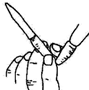 ÅųżµĪ¶Ø | ||
| C£® | 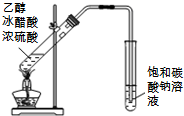 ÖĘČ”²¢ŹÕ¼Æ | D£® | 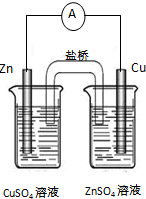 ¹¹³ÉĶŠæ |
·ÖĪö A£®¶ĮČ”µĪ¶Ø¹ÜÖŠŹż¾ŻŹ±£¬²»ÄÜø©ŹÓ¶ĮŹż£¬ŃŪ¾¦ŹÓĻßÓ¦øĆÓė°¼ŅŗĆę×īµĶµćĻąĘ½£»
B£®¼īŹ½µĪ¶Ø¹ÜÅÅĘųÅŻµÄ·½·Ø£ŗ½«¼īŹ½µĪ¶Ø¹Ü¹ÜĢåŹśÖ±£¬×óŹÖÄ“ÖøÄó×”²£Į§Ēņ£¬ĶäĒś½ŗ¹ÜŹ¹¹ÜæŚĻņÉĻ£¬ÄóŃ¹²£Į§ĒņÅųöŅŗĢ壬“ĖŹ±ĘųÅŻĘųÅŻŅ²Ėę×ÅÅųö£»
C£®µ¼¹Ü²»ÄÜÉģČėŅŗĆęŅŌĻĀ£¬·ńŌņČŻŅ×·¢Éśµ¹ĪüĻÖĻó£»
D£®ÓŅ±ßÉÕ±ÖŠŠæĄė×Ó²»»įµĆµ½µē×Ó£¬ŌņĪŽ·ØŠĪ³ÉŌµē³Ų£®
½ā“š ½ā£ŗA£®¶ĮČ”µĪ¶ØŹ±£¬ŹÓĻßÓ¦øĆÓėµĪ¶Ø¹ÜÖŠ°¼ŅŗĆęĻąĘ½£¬²»ÄÜø©ŹÓ»ņŃöŹÓ¶ĮŹż£¬·ńŌņÓ°ĻģµĪ¶Ø½į¹ū£¬¹ŹA“ķĪó£»
B£®¼īŹ½µĪ¶Ø¹ÜÅÅĘųÅŻŹ±£¬ŠčŅŖ½«¼īŹ½µĪ¶Ø¹Ü¹ÜĢåŹśÖ±£¬×óŹÖÄ“ÖøÄó×”²£Į§Ēņ£¬ĶäĒś½ŗ¹ÜŹ¹¹ÜæŚĻņÉĻ£¬ÄóŃ¹²£Į§ĒņÅųöŅŗĢ壬“ĖŹ±ĘųÅŻĘųÅŻŅ²Ėę×ÅÅųö£¬Ķ¼Ź¾²Ł×÷·½·ØŗĻĄķ£¬¹ŹBÕżČ·£»
C£®ŹÕ¼ÆŅŅĖįŅŅõ„µÄµ¼¹Ü²»ÄÜÉģČė±„ŗĶĢ¼ĖįÄĘČÜŅŗÖŠ£¬·ńŌņ»į·¢Éśµ¹ĪüĻÖĻ󣬹ŹC“ķĪó£»
D£®Šæ²»ÓėĮņĖįŠæČÜŅŗ·“Ó¦£¬¼“£ŗµē¼«Óėµē½āÖŹČÜŅŗ²»ÄÜ·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬Ōņ²»Äܹ¹³ÉŌµē³Ų£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éŹµŃé·½°øĘĄ¼Ū£¬ĪŖøßæ¼øßʵµć£¬ĢāÄæÄѶČÖŠµČ£¬Éę¼°Ōµē³ŲŌĄķ”¢õ„»Æ·“Ó¦”¢µĪ¶Ø¹ÜµÄŹ¹ÓĆ·½·Ø¼°µē½āŌĄķµČÖŖŹ¶µć£¬²ąÖŲŹµŃé²Ł×÷ŗĶŹµŃéŌĄķµÄ漲飬עŅāŹµŃé·½°øµÄ²Ł×÷ŠŌ”¢æÉŠŠŠŌ”¢ĘĄ¼ŪŠŌ·ÖĪö£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µŖŃõ»ÆŗĻĪļÓėĢ¼Ēā»ÆŗĻĪļ¾×ĻĶāĻßÕÕÉäæÉ·¢Éś·“Ó¦ŠĪ³ÉÓŠ¶¾ŃĢĪķ | |
| B£® | ĀĢÉ«»ÆѧµÄŗĖŠÄŹĒÓ¦ÓĆ»ÆѧŌĄķ¶Ō»·¾³ĪŪČ¾½ųŠŠÖĪĄķ | |
| C£® | Īķö²ÖŠŗ¬ÓŠ“óĮ泬±źµÄÖ÷ŅŖĪļÖŹŹĒ¶žŃõ»ÆĮņ | |
| D£® | ÓĆĀĮÖʵÄČŻĘ÷Ź¢×°ÅØĻõĖį£¬ŹĒŅņĪŖĀĮŗĶÅØHNO3²»·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
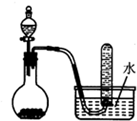
| A£® | ÅØŃĪĖįŗĶ¶žŃõ»ÆĆĢ·“Ó¦ÖĘČ”Cl2 | B£® | Ļ”ĮņĖįŗĶ“óĄķŹÆ·“Ó¦ÖĘČ”CO2 | ||
| C£® | ÅØĻõĖįÓėĶ·“Ó¦ÖĘČ”NO2 | D£® | ¶žŃõ»ÆĆĢ¹ĢĢåŗĶĖ«ŃõĖ®·“Ó¦ÖĘČ”O2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cl2-ŹŖČóµÄKIµķ·ŪŹŌÖ½-ŗģÉ« | B£® | NH3-ŹŖČóµÄĄ¶É«ŹÆČļŹŌÖ½-ŗģÉ« | ||
| C£® | NH3-ŹŖČóµÄPHŹŌÖ½-ŗģÉ« | D£® | NO2-ŹŖČóµÄKIµķ·ŪŹŌÖ½-Ą¶É« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
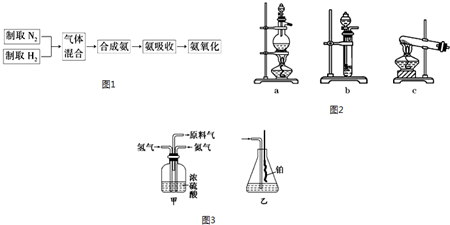
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
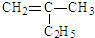
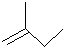
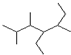 µÄĆū³Ę2£¬3£¬5-Čż¼×»ł-4-ŅŅ»łøżĶé
µÄĆū³Ę2£¬3£¬5-Čż¼×»ł-4-ŅŅ»łøżĶé ¢ŚĒāŃõøłĄė×Ó
¢ŚĒāŃõøłĄė×Ó
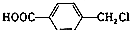 Ė®½āÖĘµĆ£¬Š“³öKŌŚÅØĮņĖį×÷ÓĆĻĀÉś³ÉµÄ¾ŪŗĻĪļµÄ½į¹¹¼ņŹ½
Ė®½āÖĘµĆ£¬Š“³öKŌŚÅØĮņĖį×÷ÓĆĻĀÉś³ÉµÄ¾ŪŗĻĪļµÄ½į¹¹¼ņŹ½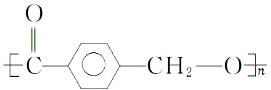 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
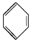 +Br2$\stackrel{FeBr_{3}}{”ś}$
+Br2$\stackrel{FeBr_{3}}{”ś}$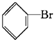 +HBr£®
+HBr£®| A£® | ¢Ł¢Ś | B£® | ¢Ū¢Ü | C£® | ¢Ł¢Ū | D£® | ¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4L±½µÄ·Ö×ÓŹżŌ¼ĪŖNAøö | |
| B£® | ³£ĪĀĻĀ£¬ŌŚ1moLC5H12ÖŠŗ¬ÓŠ¹²¼Ū¼üŹż15NA | |
| C£® | ±ź×¼×“æöĻĀ£¬17g NH3Ėłŗ¬¹²¼Ū¼üŹżĪŖNAøö | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ£¬7.0gŅŅĻ©Óė±ūĻ©µÄ»ģŗĻĪļÖŠŗ¬ÓŠĒāŌ×ӵďżÄæĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
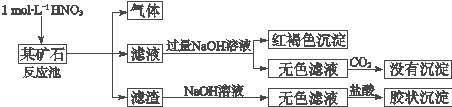
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com