
(本题16分)Ⅰ.实验室经常要制取某种气体并验证该气体的性质。
(1)下列装置适合作尾气吸收的是 (填序号)。
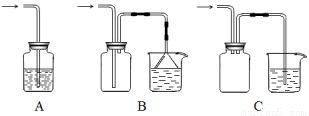
(2)向下列装置中通入气体X,A中品红溶液褪色,则X可能是___________(至少填两种)如果要证明X是SO2气体,接下来的操作是:________________________________
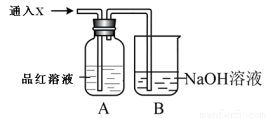
Ⅱ.实验室用FeSO4溶液和NaOH溶液反应制取Fe(OH)2,却很难看到稳定的白色沉淀。有同学设计了一种新的实验方法,能清楚看到生成白色沉淀及白色沉淀转化成红褐色沉淀的现象。请完成以下空白:
(1)取一定体积的0.1mol.L-1NaOH溶液放于烧杯中,_________后,再滴入几滴植物油;
(2)选择装置___________(填“甲”或“乙”),将(1)所得溶液加入到装置中并按图示组装好装置。
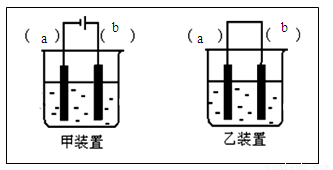
(3)在你选择的装置上标明电极材料分别为____________、________________
(4)实验中可在___________看到稳定的白色Fe(OH)2沉淀。
(5)如果要看到白色沉淀转化为红褐色沉淀的的现象,接下来的操作是______________
Ⅰ.(1)BC(2分)
(2)SO2、Cl2 (O3、ClO2等)(2分)将褪色后的溶液再加热,如果溶液又恢复成红色,则X一定为SO2 (2分)
Ⅱ.(1)加热煮沸(2分)
(2)装置甲 (2分)
(3)b-Fe (1分) a-石墨(Fe) (1分)
(4)阳极附近溶液中 (2分)
(5)将电极反向连接 (2分)
【解析】
试题分析:
Ⅰ.(1)本题答题要从防止倒吸的角度去想。
(2)能使品红褪色的可马上想到SO2,再细想一下还有Cl2、O3、ClO2,如果要证明通入的是二氧化硫,则要用试管取褪色后的溶液,用酒精灯进行加热,看是否能恢复颜色;本题答题时一定要有操作、现象、结论
Ⅱ.本题要注意目的为了制备Fe(OH)2,观察其颜色,所以关键是所用的试剂要除O2,装置要隔绝空气,(1)溶液要除氧气则用加热煮沸的方法,温度升高,气体在水是的溶解度下降(2)甲和乙装置的区别在于有无外接电源,做这种题是二选一的情况,可以用假设选用一装置,代入题意;从本题的角度,可知要产生二价铁离子,再和氢氧根离子反应,所以要选用电解池,即甲装置;b电极为阳极产生二价铁离子则为Fe,a电极为石墨;因为阳极上产生二价铁离子,所以白色沉淀在阳极的附近可观察到,如果要想白色沉淀转化为红褐色沉淀,则要加入氧化剂,从题意中不能加入,但如果将电极反接,相当于用惰性电极电解氢氧化钠溶液,即电解水,氧气就可产生了,也就实现了转化。
考点:气体收集的方法、二氧化硫、氯气等物质的漂白性、电解池原理与氢氧化亚铁的制备原理的综合运用。


科目:高中化学 来源:2013-2014广东省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.在101kPa下,1g物质完全燃烧所放出的热量叫该物质的热值,单位为kJ?mol-1
B.某放热反应在其它条件不变时,加入催化剂后反应放出的热量会减少
C.一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的
D.若一个反应的焓变ΔH=a kJ?mol-1,则其逆反应ΔH=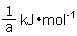
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省第一学期期终考试高一级化学科试卷乙(解析版) 题型:选择题
某溶液中的Cl-、Br-、I-的物质的量之比为2:3:4,要使溶液中Cl-、Br-、I-物质的量之比为4:3:2则通入Cl2的物质的量是原溶液中I-的量的( )
A.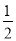 B.
B.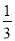 C.
C.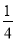 D.
D.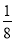
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省深圳市高考预测理综化学试卷(解析版) 题型:实验题
(本题16分)Ⅰ。某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验。
【实验1】铜与浓硫酸反应,实验装置如图所示。

实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置A中发生反应的化学方程式为 。
(2)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是 。
(3)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是 。
Ⅱ。饱和的NaHSO3溶液可以与醛发生加成反应,生成水溶性的α-羟基磺酸钠。发生的反应为:
R-CHO + NaHSO3  R-CH(OH)SO3Na
R-CH(OH)SO3Na
反应是可逆的,在通常条件下有70%--90%向正反应方向转化。
(4)利用Ⅰ中装置制取少量NaHSO3溶液,应采取措施,将装置进行部分改变。这种措施是:_____________________________________________________________________;确认有NaHSO3生成的现象是:_______________________________________.
(5)若溴苯中混有杂质乙醛,欲将此杂质除去,可采用的试剂是:__________,其分离的方法是:_____________________.
(6)若在CH3-CH(OH)SO3Na 水溶液中加入足量盐酸,有机物转化为:___________,将该转化产物分离出来的方法常用__________________.
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省深圳市高考预测理综化学试卷(解析版) 题型:选择题
X、Y、Z、W是元素周期表前四周期中的常见元素。其相关信息如下表:
元素 | 相关信息 |
X | X的一种核素的质量数为14,中子数为8 |
Y | Y与X同周期,且它的一种氧化物只能用排水法收集 |
Z | Z的单质常温下为黄绿色气体 |
W | W的原子核外电子总数是其电子层数的4倍 |
下列说法正确的是
A.原子半径:W> X>Y,离子半径:W>Z
B.氧化物对应的水化物的酸性:Z> Y>X
C.Y的最高正价含氧酸,可由它的氢化物为原料来制取
D.W的单质与X的一种氧化物不能发生置换反应
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省高考预测理综化学试卷二(解析版) 题型:选择题
现有短周期主族元素X、Y、Z、R、T。R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡。六种元素的原子半径与原子序数的关系如图所示。
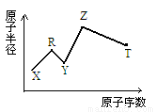
下列推断正确的是
A.离子半径:Y<Z
B.氢化物的沸点和稳定性排序 :R<Y
C.最高价氧化物对应的水化物的酸性 :T> R
D.由X、R、Y、Z四种元素组成的化合物水溶液一定显酸性
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省江门市高二调研测试理综化学试卷(解析版) 题型:填空题
3,5—二甲氧基苯酚是重要的有机合成中间体,其合成反应如下:

该反应后的混合物含有:3,5—二甲氧基苯酚、甲醇、水和HCl。
已知:甲醇、乙醚和3,5—二甲氧基苯酚的部分物理性质如下表:
物质 | 沸点/℃ | 熔点/℃ | 密度(20℃)/(g/cm3) | 溶解性 |
甲醇 | 64.7 | — | 0.7915 | 易溶于水 |
乙醚 | 34.5 | — | 0.7138 | 难溶于水 |
3,5—二甲氧基苯酚 | 172 | 36 | — | 易溶于甲醇、乙醚, 微溶于水 |
现在实验室对反应后的混合物进行分离提纯:
(1)利用与其它物质 差异较大的特点,可先用蒸馏法分离出甲醇,蒸馏操作时使用的玻璃仪器有:酒精灯、 、温度计、冷凝管 、接引管、锥形瓶。
(2)①蒸馏出甲醇后,加入乙醚进行 、 操作,有机层在分液漏斗的 层。
②双项选择:选用乙醚这种试剂的主要原因是( )
A.乙醚易挥发
B.3,5—二甲氧基苯酚在乙醚中溶解度大于在水中的溶解度
C.乙醚难溶于水
D.3,5—二甲氧基苯酚熔点较低
(3)经上述步骤分离得到的有机层再用饱和NaHCO3溶液洗涤,其目的是 。
(4)洗涤完成后,加入无水CaCl2干燥,过滤除去干燥剂,蒸馏除去乙醚,得到固体产物,为进一步提纯固体产物还要进行 操作。
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省梅州市高一下学期期中化学试卷(解析版) 题型:选择题
短周期元素甲,乙,丙,丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数和电子层数相等,则 ( )
A.原子半径:丙>丁>乙
B.单质的还原性:丁>丙>甲
C.甲,乙,丙的氧化物均为共价化和物
D.乙,丙,丁的最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省惠州市高一下学期期末考试化学(理)试卷(解析版) 题型:选择题
能将含有NaCl、AlCl3、MgCl2三种溶液一次性鉴别开来的试剂是
A. 硝酸银溶液 B.NaOH溶液 C.氨水 D.H2SO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com