
ĻĀĮŠŹĒĄūÓĆĢžC3H6ŗĻ³ÉÓŠ»śøß·Ö×ÓEŗĶĢžC6H14µÄĮ÷³ĢĶ¼£®Ēė»Ų“šŅŌĻĀĪŹĢā£ŗ
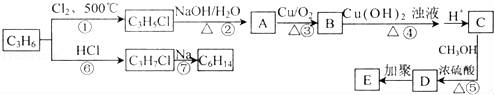
£Ø1£©¢Ł〜¢ŽÖŠŹōÓŚČ”“ś·“Ó¦µÄÓŠ £»
£Ø2£©Š“³öEµÄ½į¹¹¼ņŹ½ £»
£Ø3£©Š“³öBÓėŠĀÖĘCu£ØOH£©2Šü×ĒŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ £»
£Ø4£©DµÄĶ¬·ÖŅģ¹¹Ģåŗܶą£¬·ūŗĻĻĀĮŠĢõ¼žµÄĶ¬·ÖŅģ¹¹ĢåÓŠ ÖÖ£¬ĘäÖŠĒāŌ×ÓŗĖ“Ź²ÕńĘ×Ę×·å×īÉŁµÄ½į¹¹¼ņŹ½ĪŖ £®
¢Łŗ¬Ģ¼Ģ¼Ė«¼ü ¢ŚÄÜĖ®½ā ¢ŪÄÜ·¢ÉśŅų¾µ·“Ó¦
£Ø5£©øł¾ŻÄćĖłŃ§ÖŖŹ¶ŗĶÉĻĶ¼ÖŠĻą¹ŲŠÅĻ¢£¬ŅŌŅŅ“¼ĪŖÖ÷ŅŖŌĮĻĶعżČż²½æÉŅŌŗĻ³É»·¼ŗĶé£ØĪŽ»śŹŌ¼ĮČĪŃ”£©£¬Š“³ö·“Ó¦µÄĮ÷³ĢĶ¼£ØÓŠ»śĪļÖŹŠ“½į¹¹¼ņŹ½£©£®

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗ£ÄĻĪIJżÖŠŃ§øßŅ»ĻĀĘŚÄ©æ¼»Æѧ£ØĄķ£©ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĄė×ÓÖŠ°ė¾¶×ī“óµÄŹĒ£Ø””””£©
A. Na+ B. Mg2+ C. O2£ D. F£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗžÄĻŗāŃō°ĖÖŠø߶žµŚ¶žŃ§ĘŚĘŚÄ©æ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø12·Ö£©¹¤ŅµÉĻ²ÉÓĆŅŅ±½ĶŃĒāÖʱø±½ŅŅĻ©£¬·“Ó¦ĢåĻµĶ¬Ź±·¢ÉśĮ½²½æÉÄę·“Ó¦£¬ĘäÄÜĮæ±ä»ÆĒéæöČēĻĀ£ŗ
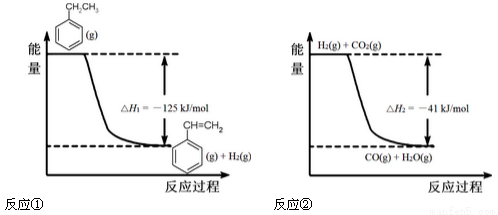
£Ø1£©×Ü·“Ó¦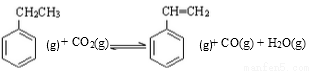 £¬ ”÷H = _________”£
£¬ ”÷H = _________”£
£Ø2£©ĻĀĮŠŠšŹö²»ÄÜĖµĆ÷·“Ó¦ĢåĻµŅŃ“ļµ½Ę½ŗāדĢ¬µÄŹĒ_______”£
A£®vÕż(CO) = vÄę(CO) B£®ĻūŗÄ1molCO2Ķ¬Ź±Éś³É1molH2O
C£®c(CO2) = c(CO) D£®»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ±£³Ö²»±ä
£Ø3£©Ä³»ÆѧŠĖȤŠ”×éÓūĢ½¾æŌŚĻąĶ¬Ń¹ĒæĢõ¼žĻĀ£¬CO2ÓĆĮæŗĶĪĀ¶ČĢõ¼ž¶ŌŅŅ±½ĶŃĒā·“Ó¦
£Ø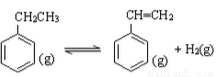 £©µÄÓ°Ļģ£¬²¢Éč¼ĘĮĖČēĻĀŹµŃé£ŗ
£©µÄÓ°Ļģ£¬²¢Éč¼ĘĮĖČēĻĀŹµŃé£ŗ

¢ŁŅŅ±½ĶŃĒā·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½ĪŖ______________”£
¢Śa=___________________”£
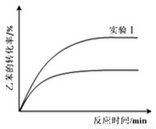
¢Ū ¾ŹµŃé²āµĆ£¬Čż×鏵ŃéÖŠŅŅ±½µÄ×Ŗ»ÆĖꏱ¼ä±ä»ÆČēÓŅĶ¼ĖłŹ¾”£ĘäÖŠĪ“ÖŖĒśĻß“ś±ķµÄŹĒŹµŃé____£ØĢī”°¢ņ”±»ņ”°III”±£©”£ĒėÓĆĘ½ŗāŅʶÆŌĄķ½āŹĶøĆĢõ¼žøıä¶ŌŅŅ±½×Ŗ»ÆĀŹ²śÉśÓ°ĻģµÄŌŅņ£ŗ______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗžÄĻŗāŃō°ĖÖŠø߶žµŚ¶žŃ§ĘŚĘŚÄ©æ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠø÷×éĄė×Ó£¬ÄÜŌŚČÜŅŗÖŠ“óĮæ¹²“ęµÄŹĒ( )
A£®Ca2+”¢Mg2+”¢Cl-”¢NO3- B£®Al3+”¢K+”¢SO42-”¢OH-
C£®Fe2+”¢H+”¢SO42-”¢NO3- D£®Na+”¢OH-”¢HCO3-”¢SO42-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗžÄĻŗāŃō°ĖÖŠø߶žµŚ¶žŃ§ĘŚĘŚÄ©æ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÓŠŅ»ÖÖŅųŠæµē³Ų£¬Ęäµē¼«·Ö±šĪŖAg2OŗĶZnO£¬µē½āÖŹČÜŅŗĪŖKOH”¢µē¼«·“Ó¦Ź½·Ö±šĪŖ£ŗZn+2OH-- 2e-=ZnO+H2O, Ag2O+H2O+2e-=2Ag+2OH-,øł¾ŻÉĻŹö·“Ó¦Ź½£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
A£®ZnŹĒÕż¼«£¬Ag2OŹĒøŗ¼«
B£®Ź¹ÓĆ¹ż³ĢÖŠ£¬µē×ÓÓÉAg2O¼«¾ĶāĀ·Į÷ĻņZn¼«
C£®Ź¹ÓĆ¹ż³ĢÖŠ£¬µē¼«øŗ¼«ĒųČÜŅŗµÄpH¼õŠ”
D£®Znµē¼«·¢Éś»¹Ō·“Ó¦£¬Ag2Oµē¼«·¢ÉśŃõ»Æ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”ø߶žĻĀµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ņ»¶ØĮæµÄFeŗĶFe2O3»ģŗĻĪļĶ¶Čė2mol/L250mLµÄHNO3ČÜŅŗÖŠ£¬·“Ó¦ĶźČ«ŗó£¬ĪŽ¹ĢĢåŹ£Óą£¬Éś³É2.24L£Ø±ź×¼×“æö£©NOĘųĢ壬ŌŁĻņ·“Ó¦ŗóČÜŅŗÖŠ¼ÓČė1mol/LµÄNaOHČÜŅŗ£¬ŅŖŹ¹ĢśŌŖĖŲČ«²æ³ĮµķĻĀĄ“£¬Ėł¼ÓNaOHČÜŅŗµÄĢå»ż×īÉŁŹĒ£Ø £©
A£®400mL B£®450mL C£®500mL D£®ĪŽ·ØČ·¶Ø
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”¾Å½ŹŠø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
Ä³ŃŠ¾æŠŌѧĻ°Š”×éĪŖČ·¶ØŅ»ÖÖ“ÓĆŗÖŠĢįČ”µÄŅŗĢ¬ĢžXµÄ½į¹¹£¬¶ŌĘä½ųŠŠĢ½¾æ£®
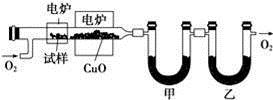
²½ÖčŅ»£ŗÕāÖÖĢ¼Ēā»ÆŗĻĪļÕōĘųĶعżČȵÄŃõ»ÆĶ£Ø“߻ƼĮ£©£¬Ńõ»Æ³É¶žŃõ»ÆĢ¼ŗĶĖ®£¬ŌŁÓĆ×°ÓŠĪŽĖ®ĀČ»ÆøĘŗĶ¹ĢĢåĒāŃõ»ÆÄʵÄĪüŹÕ¹ÜĶźČ«ĪüŹÕ£®2.12gÓŠ»śĪļXµÄÕōĘųŃõ»Æ²śÉś7.04g¶žŃõ»ÆĢ¼ŗĶ1.80gĖ®£®
²½Ö趞£ŗĶعżŅĒĘ÷·ÖĪöµĆÖŖXµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ106£®
²½ÖčČż£ŗÓĆŗĖ“Ź²ÕńŅĒ²ā³öXµÄ1HŗĖ“Ź²ÕńĘ×ÓŠ2øö·å£¬ĘäĆ껿֮±ČĪŖ2£ŗ3£®ČēĶ¼¢ń£®
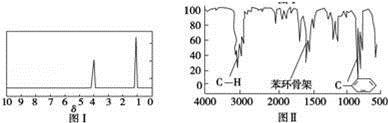
²½ÖčĖÄ£ŗĄūÓĆŗģĶā¹āĘ×ŅĒ²āµĆX·Ö×ÓµÄŗģĶā¹āĘ×ČēĶ¼¢ņ£®
ŹŌĢīæÕ£ŗ
£Ø1£©XµÄ·Ö×ÓŹ½ĪŖ £»XµÄĆū³ĘĪŖ £®
£Ø2£©²½Ö趞֊µÄŅĒĘ÷·ÖĪö·½·Ø³ĘĪŖ £®
£Ø3£©Š“³öXÓė×ćĮæÅØĻõĖįŗĶÅØĮņĖį»ģŗĻĪļ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ £®
£Ø4£©Š“³öX·ūŗĻĻĀĮŠĢõ¼žµÄĶ¬·ÖŅģ¹¹Ģå½į¹¹¼ņŹ½ £®
¢Ł·¼ĻćĢž ¢Ś±½»·ÉĻŅ»ĀČ“śĪļÓŠČżÖÖ
£Ø5£©XŅŌ“×ĖįĪŖČܼĮŌŚ“߻ƼĮ×÷ÓĆĻĀÓĆŃõĘųŃõ»ÆµĆµ½ĮķŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻPTA£¬²éŌÄ׏ĮĻµĆÖŖPTAµÄČܽā¶Č£ŗ25”ꏱ0.25g”¢50”ꏱ0.97g”¢95”ꏱ7.17g£®µĆµ½µÄ“Ö²śĘ·ÖŠÓŠ²æ·Ö²»ČÜŠŌŌÓÖŹ£¬Ēė¼ņŹöŹµŃéŹŅÖŠĢį“æPTAµÄŹµŃé·½°ø£ŗ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”¾Å½ŹŠø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ö»ŗ¬C”¢H”¢OČżÖÖŌŖĖŲµÄÓŠ»śĪļ£¬ŌŚæÕĘųÖŠČ¼ÉÕŹ±ĻūŗĵÄO2ŗĶÉś³ÉµÄCO2µÄĢå»ż±ČŹĒ1£ŗ2£¬ŌŚÕāĄąÓŠ»śĪļÖŠ£Ø £©
A£®Ļą¶Ō·Ö×ÓÖŹĮæ×īŠ”µÄ»ÆŗĻĪļ·Ö×ÓŹ½ŹĒCH2O
B£®Ļą¶Ō·Ö×ÓÖŹĮæ×īŠ”µÄ»ÆŗĻĪļ·Ö×ÓŹ½ŹĒC2H2O
C£®ŗ¬ĻąĶ¬Ģ¼Ō×ÓŹżµÄø÷»ÆŗĻĪļ£¬ĘäĻą¶Ō·Ö×ÓÖŹĮæÖ®²īŹĒ16µÄÕūŹż±¶
D£®ŗ¬ĻąĶ¬Ģ¼Ō×ÓŹżµÄø÷»ÆŗĻĪļ£¬ĘäĻą¶Ō·Ö×ÓÖŹĮæÖ®²īŹĒ18µÄÕūŹż±¶
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗÓÄĻÖ£ÖŻĶā¹śÓļѧŠ£ø߶žÉĻæŖŃ§æ¼ŹŌ»Æѧ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ĆŗČ¼ÉÕÅŷŵÄŃĢĘųŗ¬ÓŠSO2ŗĶNOx£¬ŠĪ³ÉĖįÓź”¢ĪŪČ¾“óĘų£¬²ÉÓĆNaClO2ČÜŅŗ×÷ĪŖĪüŹÕ¼ĮæÉĶ¬Ź±¶ŌŃĢĘų½ųŠŠĶŃĮņ”¢ĶŃĻõ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©NaClO2µÄ»ÆѧĆū³ĘĪŖ_______”£
£Ø2£©ŌŚ¹ÄÅŻ·“Ó¦Ę÷ÖŠĶØČėŗ¬ÓŠSO2ŗĶNOµÄŃĢĘų£¬·“Ó¦ĪĀ¶ČĪŖ323 K£¬NaClO2ČÜŅŗÅضČĪŖ5”Į10£3mol”¤L£1”£·“Ó¦Ņ»¶ĪŹ±¼äŗóČÜŅŗÖŠĄė×ÓÅØ¶ČµÄ·ÖĪö½į¹ūČēĻĀ±ķ”£
Ąė×Ó | SO42£ | SO32£ | NO3£ | NO2£ | Cl£ |
c/£Ømol”¤L£1£© | 8.35”Į10£4 | 6.87”Į10£6 | 1.5”Į10£4 | 1.2”Į10£5 | 3.4”Į10£3 |
¢ŁŠ“³öNaClO2ČÜŅŗĶŃĻõ¹ż³ĢÖŠÖ÷ŅŖ·“Ó¦µÄĄė×Ó·½³ĢŹ½ ”£Ōö¼ÓŃ¹Ē棬NOµÄ×Ŗ»ÆĀŹ £ØĢī”°Ģįøß”±”¢”°²»±ä”±»ņ”°½µµĶ”±£©”£
¢ŚĖę×ÅĪüŹÕ·“Ó¦µÄ½ųŠŠ£¬ĪüŹÕ¼ĮČÜŅŗµÄpHÖš½„ £ØĢī”°Ōö“ó”±”°²»±ä”±»ņ”°¼õŠ””±£©”£
¢ŪÓÉŹµŃé½į¹ūæÉÖŖ£¬ĶŃĮņ·“Ó¦ĖŁĀŹ ĶŃĻõ·“Ó¦ĖŁĀŹ£ØĢī”°“óÓŚ”±»ņ”°Š”ÓŚ”±£©”£ŌŅņŹĒ³żĮĖSO2ŗĶNOŌŚŃĢĘųÖŠµÄ³õŹ¼ÅØ¶Č²»Ķ¬£¬»¹æÉÄÜŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com