
| A. | 0.58 g/L | B. | 0.29 g/L | C. | 1.16 g/L | D. | 0.714 g/L |
分析 根据n=$\frac{m}{M}$计算甲烷物质的量,13g某气体与8g CH4的分子数相同,则二者物质的量相等,根据V=nVm计算该气体的体积,再根据ρ=$\frac{m}{V}$计算气体的密度.
解答 解:8g CH4的物质的量为$\frac{8g}{16g/mol}$=0.5mol,13g某气体与8g CH4的分子数相同,则二者物质的量相等,标况下该气体的体积为0.5mol×22.4L/mol=11.2L,则该条件下气体的密度为$\frac{13g}{11.2L}$=1.16 g/L,
故选:C.
点评 本题考查物质的量有关计算,比较基础,可以计算先气体的摩尔质量,再根据ρ=$\frac{M}{{V}_{m}}$计算.


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 活化分子间的碰撞一定是有效碰撞 | |
| B. | 活化分子具有的能量是活化能 | |
| C. | 活化分子的总数越多,反应速率越快 | |
| D. | 单位时间内有效碰撞次数越多,反应速率越快 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
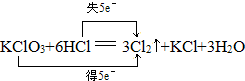 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N×10-2 mol/L | B. | $\frac{N}{1.204×1{0}^{22}}$ mol/L | ||
| C. | $\frac{N}{6.02×1{0}^{21}}$mol/L | D. | $\frac{N}{6.02×1{0}^{25}}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA | |
| B. | 常温常压下,1.7gH2O2中含有的电子数为0.8NA | |
| C. | 通常状况下,2.24LCO2和CO中所含分子数为0.1NA | |
| D. | 23gNO2和N2O4的混合气所含原子数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纳米铜是一种新型化合物 | |
| B. | 纳米铜颗粒比普通铜具有更强的化学活性 | |
| C. | 纳米铜粒子大小介于1~100 nm | |
| D. | 利用丁达尔现象可区别纳米铜和普通铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子所以能导电 | |
| B. | 二氧化硫的水溶液能导电,所以二氧化硫是电解质 | |
| C. | 硫酸钡难溶于水,但硫酸钡属于电解质 | |
| D. | 液态氯化氢不导电,所以氯化氢是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com