
【题目】关于ag氢气和bg氦气的下列说法正确的是( )
A. 同温、同压下,氢气与氦气的体积比为a:2b
B. 同温、同压下,若a=b,则氢气与氦气的物质的量之比为2:1
C. 体积相同时,氢气的质量一定小于氦气的质量
D. 同温同压下,若两者的体积相等,则其原子数也相等
【答案】B
【解析】A. 氢气的摩尔质量为2g/mol,氦气的摩尔质量为4g/mol,氢气与氦气的物质的量之比为2a:b,同温、同压下,氢气与氦气的体积比等于物质的量之比为2a:b,故A错误;B. 同温、同压下,若a=b,氢气的摩尔质量为2g/mol,氦气的摩尔质量为4g/mol,氢气与氦气的摩尔质量之比为1:2,所以氢气与氦气的物质的量之比为2:1,故B正确;C. 温度和压强不确定,所以体积相同时,氢气的质量不一定小于氦气的质量,故C错误;D. 同温同压下, ![]() =
=![]() =
=![]() ,若两者的体积相等,则它们的分子数相等。由于氢气分子是双原子分子,而氦气分子是单原子分子,所以它们的原子数不相等,故D错误。故选B。
,若两者的体积相等,则它们的分子数相等。由于氢气分子是双原子分子,而氦气分子是单原子分子,所以它们的原子数不相等,故D错误。故选B。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】海水的综合利用可以制备金属钠和镁,其流程如下图所示:

下列说法不正确的是( )
A. 要检验母液中是否含氯离子应当用硝酸酸化的硝酸银溶液进行实验
B. 上述流程MgCl2制取Mg的反应中,MgCl2既是氧化剂又是还原剂
C. 上述流程中的变化都属于化学变化
D. 上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg:2++Ca(OH)2=Mg(OH)2+Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据下列图示,写出反应的热化学方程式。
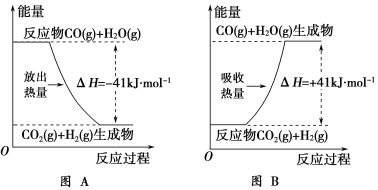
A.___________________________________。
B.___________________________________。
(2)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式为___________________。
(3)如图是598 K时,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为_______________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 凡有能量变化的过程都是化学变化
B. 放热反应可能需要加热才能进行
C. 吸热反应只能在加热条件下才能进行 .
D. 天然气在空气中燃烧时,化学能全部转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸乙二脂(D)可由石油气裂解得到的烯烃合成。回答下列问题
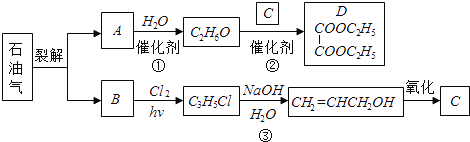
(1)B和A为同系物,B的结构简式为_______________。
(2)反应①的化学方程式为______________, 其反应类型为________________。
(3)反应③的反应类型为_________________。
(4)C的结构简式为_______________。
(5)反应②的化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置进行实验,甲、乙两池中均为1 mol·L-1的AgNO3溶液,A、B均为Ag电极。实验开始时先闭合K1,断开K2。一段时间后,断开K1,闭合K2,形成浓差电池,电流表指针偏转(Ag+浓度越大氧化性越强)。下列说法不正确的是( )
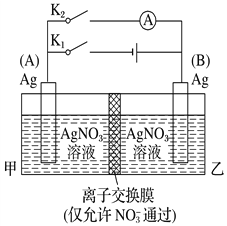
A. 闭合K1,断开K2后,A电极增重
B. 闭合K1,断开K2后,乙池溶液浓度上升
C. 断开K1,闭合K2后,A电极发生氧化反应
D. 断开K1,闭合K2后,NO![]() 向B电极移动
向B电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】COS 、H2S是许多煤化工产品的原料气。已知
Ⅰ.COS(g)+H2(g)![]() H2S(g)+CO(g) △H=X kJ·mol-1;
H2S(g)+CO(g) △H=X kJ·mol-1;
Ⅱ.CO(g)+H2O(g)![]() CO2(g)+H2(g) △H =-42 kJ·mol-1;
CO2(g)+H2(g) △H =-42 kJ·mol-1;
(1)断裂1 mol分子中的化学键所需吸收的能量如下表所示:
分子 | COS(g) | H2(g) | CO(g) | H2S(g) | H2O(g) | CO2(g) |
能量/kJ·mol-1 | 1319 | 442 | 1076 | 678 | 930 | 1606 |
X=___________。
(2)向10 L容积不变的密闭容器中充入1 mol COS(g)、1 mol H2(g)和1 mol H2O(g),进行上述两个反应,在T10C时达到平衡,体系内CO的体积分数为5%(如下图M点)。

请回答下列问题:
①请在图中画出以M为起点,从T1℃开始升温过程中CO的平衡体积分数随温度变化的曲线。_____
②T1℃时,测得平衡时体系中COS的物质的量为0.80 mol,则平衡时H2O的转化率为_________。
(3)现有两个相同的2 L恒容绝热(与外界没有热量交换)密闭容器M、N,在M中充入1 mol CO和1 mol H2O,在N中充入1 mol CO2和1 mol H2,均在700 ℃下开始按Ⅱ进行反应。达到平衡时,下列说法正确的是_______。
A.容器M、N中正反应速率相同
B.容器M中CO的物质的量比容器N中的多
C.容器M、N中反应的平衡常数相同
D.容器M中CO的转化率与容器N中CO2的转化率之和小于1
(4)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
H2CO3 | H2S | |
Ka1 | 4.4×10-7 | 1.3×10-7 |
Ka2 | 4.7×10-11 | 7.1×10-15 |
煤的气化过程中产生的H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为
______________________________________;常温下,用100mL 0.1mol·L-1NaOH溶液吸收224mL(标况)H2S气体,反应后离子浓度从大到小顺序为_____________________。
(5)25℃时,用Na2S沉淀Cu2+、Sn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示:

①25℃时Ksp(CuS)=__________________。
②25℃时向50.0mL Sn2+、Cu2+浓度均为0.01mol·L-1的混合溶液中逐滴加入Na2S溶液到50.0mL时开始生成SnS沉淀,此时溶液中Cu2+浓度为__________mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com