
四种短周期元素,乙原子有三个电子层,第一层与最外层电子数相等;甲原子的核外电子数比乙原子核外电子数少1;丙原子的最外层电子数是次外层电子数的2倍;丁原子核电荷数比丙原子核电荷数多2。请回答:
(1)甲是 元素(填元素符号),甲的单质与水反应的化学方程式为:
;
(2)乙是 元素(填元素符号),原子结构示意图为______________________;
(3)丙是 元素(填元素名称),它在元素周期表中的位置 ;
(4)丁是 元素(填元素名称),甲与丁两种元素可组成的物质有
、 。(填化学式)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是
A.原子半径:A>B>C>D B.离子半径:D(n+1)->Cn->B(n+1)+>An+
C.原子序数:b>a>c>d D.金属性:B>A,气态氢化物稳定性:D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
Y元素最高正价与最低负价的绝对值之差是4;Y元素与M元素形成离子化合物,并在水中电离出电子层结构相同的离子,该化合物是( )
A.KCl B.Na2S C.Na2O D.K2S
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.煤焦油、石油、花生油都属于烃
B.蛋白质、脂肪、葡萄糖在一定条件下都能水解
C.甲烷、乙烯、苯都可通过石油分馏得到
D.乙醇既能与有机化合物反应又能与无机化合物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成.为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
已知:①NiCl2易溶水,Fe3+不能氧化Ni2+
②该温度下一些难溶物的Ksp及沉淀析出的理论pH如下表所示:
| Ksp | 开始沉淀pH | 沉淀完全pH |
| |
| Al(OH)3 | 1.9×10-33 | 3.43 | 4.19 | |
| Fe(OH)3 | 3.8×10-38 | 2.53 | 2.94 | |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 | |
| NiC2O4 | 4.0×10-10 | —— | —— |
回答下列问题:
(1)该工艺流程中多次重复利用的一种实验基本操作是 。
(2)步骤①所留残渣的主要成分为 (填物质名称)
(3)根据上表数据判断步骤②依次析出沉淀Ⅱ______和沉淀Ⅲ______(填化学式),
控制两种沉淀析出可利用 。
A.pH试纸 B.石蕊指示剂 C.pH计
(4)已知实验温度时的溶解度:NiC2O4>NiC2O4•H2O>NiC2O4•2H2O,则步骤③的化学反应方程式是 。
(5)C可被E氧化,写出步骤④的离子反应方程式 。
(6)FeCl3和AlCl3 的混合溶液中加入NaOH溶液,若Fe(OH)3和Al(OH)3同时存在,则c(Fe3+)/c(Al3+)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
A.离子化合物不一定含有金属元素 B.分子晶体中一定含有共价键
C.原子晶体熔化时破坏共价键 D.离子化合物中可以含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
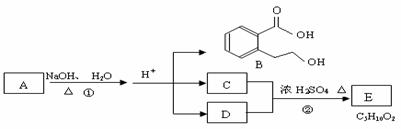 下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应;C和D的相对分子质量相等,且E为无支链的化合物。根据下图回答问题:
下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应;C和D的相对分子质量相等,且E为无支链的化合物。根据下图回答问题:
(1)C分子中的官能团名称是 ______________;化合物B不能发生的反应是 (填字母序号):
a 加成反应 b取代反应 c消去反应 d酯化反应 e水解反应 f 置换反应
(2)反应②的化学方程式是_____ _。
(3)反应②实验中加热的目的是(从速率和平衡两个角度分析)
(4) A的结构简式是 __________________ 。
(5)同时符合下列三个条件的B的同分异构体的数目有 个。
I.含有间二取代苯环结构 Ⅱ.属于非芳香酸酯 Ⅲ.与 FeCl3 溶液发生显色反应。
写出其中任意一个同分异构体的结构简式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com