
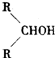
 最难
最难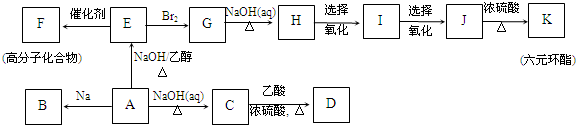
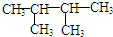 ,K为
,K为 ;
;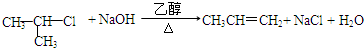 ;G→H
;G→H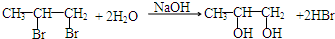 ;
;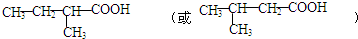 .
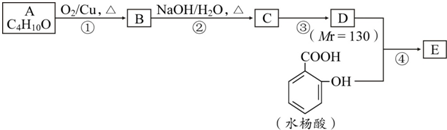
. 分析 氯代烃A,其相对分子质量为78.5,则A的分子式为C3H7Cl,A与钠发生题中信息中的反应生成B,B与氯气反应生成的一氯代物有两种,则A为CH3CHClCH3,B为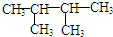 ,A在氢氧化钠醇溶液中发生消去反应生成E为CH2=CHCH3,E发生加聚反应得F为
,A在氢氧化钠醇溶液中发生消去反应生成E为CH2=CHCH3,E发生加聚反应得F为 ,E与溴发生加成反应得G为CH2BrCHBrCH3,G水解得H为CH2OHCHOHCH3,H选择氧化得I为CH3CHOHCHO,I选择氧化得J为CH3CHOHCOOH,J在浓硫酸加热条件下得六元环酯K为
,E与溴发生加成反应得G为CH2BrCHBrCH3,G水解得H为CH2OHCHOHCH3,H选择氧化得I为CH3CHOHCHO,I选择氧化得J为CH3CHOHCOOH,J在浓硫酸加热条件下得六元环酯K为 ,A碱性水解得 C为CH3CHOHCH3,C与乙酸发生酯化反应得D为CH3COOCH(CH3)2,据此答题.
,A碱性水解得 C为CH3CHOHCH3,C与乙酸发生酯化反应得D为CH3COOCH(CH3)2,据此答题.
解答 解:氯代烃A,其相对分子质量为78.5,则A的分子式为C3H7Cl,A与钠发生题中信息中的反应生成B,B与氯气反应生成的一氯代物有两种,则A为CH3CHClCH3,B为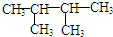 ,A在氢氧化钠醇溶液中发生消去反应生成E为CH2=CHCH3,E发生加聚反应得F为
,A在氢氧化钠醇溶液中发生消去反应生成E为CH2=CHCH3,E发生加聚反应得F为 ,E与溴发生加成反应得G为CH2BrCHBrCH3,G水解得H为CH2OHCHOHCH3,H选择氧化得I为CH3CHOHCHO,I选择氧化得J为CH3CHOHCOOH,J在浓硫酸加热条件下得六元环酯K为
,E与溴发生加成反应得G为CH2BrCHBrCH3,G水解得H为CH2OHCHOHCH3,H选择氧化得I为CH3CHOHCHO,I选择氧化得J为CH3CHOHCOOH,J在浓硫酸加热条件下得六元环酯K为 ,A碱性水解得 C为CH3CHOHCH3,C与乙酸发生酯化反应得D为CH3COOCH(CH3)2,
,A碱性水解得 C为CH3CHOHCH3,C与乙酸发生酯化反应得D为CH3COOCH(CH3)2,
(1)根据上面的分析可知,A的分子式为C3H7Cl,A→C的反应类型为取代反应,E→F的反应类型加聚反应,
故答案为:C3H7Cl;取代反应;加聚反应;
(2)根据上面的分析可知,B为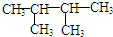 ,K为
,K为 ,
,
故答案为: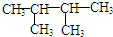 ;
;  ;
;
(3)A→E的反应方程式为 ,G→H的反应方程式为
,G→H的反应方程式为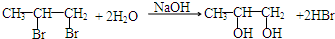 ,
,
故答案为: ;
; 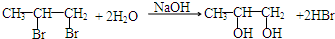 ;
;
(4)D为CH3COOCH(CH3)2,D的同分异构体属于羧酸的有四种,其中有2个-CH3基团的有两种,则其结构简式为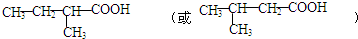 ,
,
故答案为: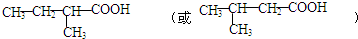 .
.
点评 本题考查有机物的推断与合成,难度较大,是对有机物知识的综合考查,综合性较强,能较好的考查学生的阅读、分析与思维能力,(4)为本题的易错点.


科目:高中化学 来源: 题型:选择题
| A. | 常温下①溶液显碱性,其主要原因为:CO32-+H2O=HCO3-+OH- | |
| B. | 可用澄清石灰水来鉴别①和②两种无色溶液 | |
| C. | 泡沫灭火器中用硫酸铝溶液和②混合快速产生CO2的反应原理为:Al3++3HCO3-=Al(OH)3↓+3CO2↑ | |
| D. | 无论①和②以何种比例、何种浓度混合,都一定有:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 28g氮气所含有的原子数目为NA | |
| B. | 常温常压下,32gO2含有的O原子数为NA | |
| C. | 1mol甲烷的质量与NA个甲烷分子的质量之和相等 | |
| D. | 标准状况下,22.4L 甲烷和乙炔的混合气体所含的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

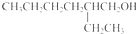 .
.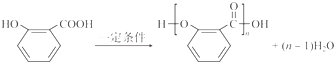 .
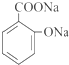
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
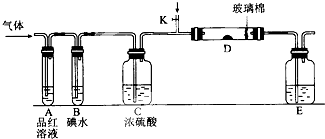 某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究S02和Cl2的性质.
某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究S02和Cl2的性质.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知如图装置的甲、乙两室内装入液体的体积相同.请回答下列问题:
已知如图装置的甲、乙两室内装入液体的体积相同.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com