
���仯�����ڿ��м������о�������Ҫ�����á�
��1������P(s)��Cl2(g)������Ӧ����PCl3(g)PCl5(g)����Ӧ�������£�
2P(s) + 3Cl2(g) = 2PCl3(g) ��H=��612kJ/mol
2P(s) + 5Cl2(g) = 2PCl5(g) ��H=��798kJ/mol
��̬ PCl5������̬PCl3��Cl2���Ȼ�ѧ����ʽΪ________��
��2��һ���¶��£����������������Ϊ2.0L�������з�����Ӧ��PCl5��g�� PCl3��g��+Cl2��g��
PCl3��g��+Cl2��g��
��� | �¶ȣ��棩 | ��ʼ/mol | ƽ��/mol | �ﵽƽ������ʱ��/s | |
PCl5��g�� | PCl3��g�� | Cl2��g�� | |||
I | 320 | 0.40 | 0.10 | 0.10 | t1 |
II | 320 | 0.80 | t2 | ||
III | 410 | 0.40 | 0.15 | 0.15 | t3 |
��ƽ�ⳣ��K����ҺII____��ҺIII���>����=����<����
�ڷ�Ӧ�ﵽƽ��ʱ��PCl3��ת���ʣ�����II_____����I���>����=����<����
��3�������ᣨH2PO5����������NaOH��Һ��Ӧ����Na2HPO3�����Na2HPO3��ҺҲ�ɵõ����[�ᣬװ��ʾ��ͼ��ͼ��
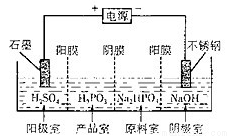
�����ĵ缫��ӦʽΪ_______����Ʒ���з�Ӧ�����ӷ���ʽΪ__________��
��4��һ���¶��£�Ksp[Mg3(PO4)2]=6.0��10-29��Ksp[Ca3(PO4)2]=6.0��10-26��Ũ�Ⱦ�Ϊ0.20 mol��L-1��MgCl2��CaCl2�����Һ����μ���Na3PO3��������________�������ѧʽ�����������Һ����һ�ֽ��������ӳ�����ȫ��Ũ��С��105mol/L��ʱ����Һ�е���һ�ֽ��������ӵ����ʵ���Ũ��c= ______mol/L

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ���ӱ�ʡ2016-2017ѧ���һ��ѧ�ڿ�ѧ���Ի�ѧ�Ծ� ���ͣ�ѡ����
�ڢ�Al ��Al2O3 ��Al(OH)3 ��NaHCO3���������У����������ᷴӦ���ܺ��������Ʒ�Ӧ�Ļ�������
A. �ڢۢ� B. �٢ڢۢ� C. �٢ۢ� D. �٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���½�����ũ��ʦ��ɽ��ѧ��һ��ѧ��ѧǰ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����״̬�����ʣ����ܵ��������ڵ���ʵ��ǣ� ��
A. MgCl2���� B. NaCl��Һ C. Һ̬�Ȼ��� D. ���ڵ�KOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��㶫ʡ�����и�һ��ѧ������ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ����
A. ̼�������Һ�м�������������������Һ��Ca2����2HCO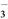 ��2OH��= CaCO3����CO
��2OH��= CaCO3����CO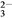 ��2H2O
��2H2O
B. �����ʯ��ˮ��ϡ���ᷴӦ��Ca(OH)2 + 2H+ = Ca2+ + 2H2O
C. ������������Һ�е���������������Һ��Al3+ +3OH- = Al(OH)3��
D. ����CuSO4��Һ��Ӧ��2Na + Cu2+ = 2Na+ + Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��㶫ʡ�����и�һ��ѧ������ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ��������¹ʴ����У�������ȷ����
A. ��ϡ������ϴ����ɫ��Ӧ�IJ�˿
B. ������������ҺҪ����������ϡ���ᱣ��
C. ��ʣ�Ľ�����Ҫ�Ż�ԭ�Լ�ƿ�У��������ⶪ��
D. �����������Ż�����øɷۣ���NaHCO3)��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ����2���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
CuI��һ�ֲ�����ˮ�İ�ɫ���壬�����ɷ�Ӧ2Cu2��+4I-=2CuI��+I2���õ�������ʯīΪ��������CuΪ�������KI��Һ��ͨ��ǰ����Һ�м���������̪�͵�����Һ����ʼ������������Һ�ʺ�ɫ������������Һ����ɫ������Щ�������ȷ������
������2I--2e-= H2����I2�����۱���
������2H2O--4e-=O2��+4H+��O2��I-����ΪI2��I2�����۱���
������2H2O+2e-= H2��+OH-��ʹc��OH-��>c��H+��
������2Cu-4e-+4I-=2CuI+I2��I2�����۱���
A. �٢� B. �٢� C. �٢� D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ����2���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
������̼�IJ����������������ҹ���Դ�����һ����Ҫս�Է���չ��һ����Ҫ�����˲�ҵ��
��1����֪��CH4��CO��H2��ȼ���ȷֱ�Ϊ890 kJ•mol��1��283 kJ•mol��1��285.8 kJ•mol��1���������з�Ӧ�ķ�Ӧ�ȡ�CO2��g��+CH4��g���� 2CO��g��+ 2H2��g�� ��H��____kJ•mol��1��
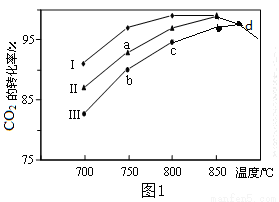
��2�����÷����е�CO2Ϊԭ����ȡ�״�����Ӧ����ʽΪ��CO2��3H2 CH3OH��H2O����������ͬ���ü״��ϳɷ�Ӧ�ڲ�ͬ�������������·�Ӧ��ͬʱ���CO2��ת�����淴Ӧ�¶ȵı仯��ͼ����ʾ��
CH3OH��H2O����������ͬ���ü״��ϳɷ�Ӧ�ڲ�ͬ�������������·�Ӧ��ͬʱ���CO2��ת�����淴Ӧ�¶ȵı仯��ͼ����ʾ��
�ٸ÷�Ӧ�Ħ�H______0�������������
��d�㲻ͬ��������������CO2��ת������ͬ��ԭ����_______________��

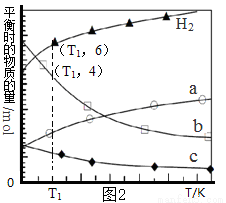
��3���ö�����̼���������ϳɵ�̼ϩ������ʼʱ��0.1MPa��n��H2����n��CO2��=3��1��Ͷ�ϱȳ��뷴Ӧ���У�������Ӧ��2CO2��g��+6H2��g�� C2H4��g��+4H2O��g����H����ͬ�¶���ƽ��ʱ��������̬���ʵ����ʵ�����ͼ2��ʾ��
C2H4��g��+4H2O��g����H����ͬ�¶���ƽ��ʱ��������̬���ʵ����ʵ�����ͼ2��ʾ��
�ٸ÷�Ӧ��__________�Է����У�����¡����¡�����
��c������������_______________��
��T1�¶��µ�ƽ��ת����Ϊ__________________���������ʼ״̬��ƽ��ʱ�����ƽ����Է�����������İٷ���Ϊ_______________��������λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ������ѧ���ڳ����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�����ָ����Һ������Ũ�ȹ�ϵ��ȷ���ǣ� ��
A. 0.1mol ��L��1NH4Cl��Һ�У�c(Cl��)>c(NH4+)>c(H+)>c(OH��)
B. 0.1mol ��L��1Na2CO3��Һ�У�c(OH��)��c(H+)+c(HCO3��)+ c(H2CO3)
C. ����ˮ�м���NaOH��Һ��pH��7��������Һ�У�c(Na+)��c(ClO��)��c(Cl��)��c(OH��)
D. 0.2mol ��L��1H2C2O4�����ᣩ��0.1mol ��L��1 NaOH��Һ�������ϵ���Һ�У�2[c(H+)-c(OH��)]��3c(C2O42��)-c(H2C2O4)+ c(HC2O4��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�ϲ��и�һ��ѧ�ڷְ�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ij��Һ�м��뺬Fe2������Һ�������Ա仯�����ٵ���������ˮ�����Һ��ɺ�ɫ�������н��۴������(����)
A. ����Һ��һ������SCN�� B. �����ԣ�Fe3����Cl2
C. Fe2����SCN�������γɺ�ɫ���� D. Fe2��������ΪFe3��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com