
| A. | 质量数为198 | B. | 中子数为82 | ||
| C. | 与${\;}_{58}^{142}$Ce为同素异形体 | D. | Ce元素相对原子质量为140 |
分析 A.B.根据原子符号的含义以及质量数=质子数+中子数,质子数=核外电子数来解答.
C.同一元素形成的不同单质为同素异形体;根据质子数相同,中子数不同原子,属于同位素;
D.元素的相对原子质量是指元素的平均相对原子质量,它是根据天然同位素原子所占的原子个数百分比和其相对原子质量计算出的平均值;
解答 解:A.${\;}_{58}^{140}$Ce的质量数为140,故A错误;
B.${\;}_{58}^{140}$Ce的质子数为58,质量数为140,中子数为140-58=82,故B正确;
C.${\;}_{58}^{140}$Ce与${\;}_{58}^{142}$Ce的质子数相同,中子数不同,属于同位素,故C错误;
D.根据一种核素的相对原子质量,无法求出Ce元素相对原子质量,故D错误;
故选B.
点评 本题主要考查了原子符号的含义以及质量数=质子数+中子数,质子数=核外电子数,题目较简单.


科目:高中化学 来源: 题型:解答题
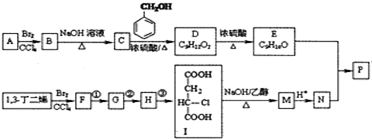
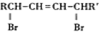 (R、R′表示烃基)
(R、R′表示烃基) (其中R1~R2表示氢或烃基)
(其中R1~R2表示氢或烃基) .
. .
. (其中任一种).
(其中任一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.02mol/(L•s) | ||
| C. | v(C)=0.01mol/(L•s) | D. | v(D)=0.1mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥ | B. | ②③⑤ | C. | ①②⑤⑥ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCl2溶液 | B. | AgNO3溶液 | C. | H2SO4溶液 | D. | 稀盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com