
 ŗĻ³É°±¹¤Ņµ¶Ō¹śĆń¾¼ĆŗĶÉē»į·¢Õ¹¾ßÓŠÖŲµÄŅāŅ壮¶ŌÓŚĆܱÕČŻĘ÷ÖŠµÄ·“Ó¦£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg£©£ØÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦£©£¬673K”¢30MPa ĻĀ£¬n£ØNH3£©ŗĶ n£ØH2£©Ėꏱ¼ä t ±ä »ÆµÄ¹ŲĻµŹ¾ŅāĶ¼ČēĶ¼ĖłŹ¾£®ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø””””£©
ŗĻ³É°±¹¤Ņµ¶Ō¹śĆń¾¼ĆŗĶÉē»į·¢Õ¹¾ßÓŠÖŲµÄŅāŅ壮¶ŌÓŚĆܱÕČŻĘ÷ÖŠµÄ·“Ó¦£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg£©£ØÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦£©£¬673K”¢30MPa ĻĀ£¬n£ØNH3£©ŗĶ n£ØH2£©Ėꏱ¼ä t ±ä »ÆµÄ¹ŲĻµŹ¾ŅāĶ¼ČēĶ¼ĖłŹ¾£®ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | c µć“¦Õż·“Ó¦ĖŁĀŹŗĶÄę·“Ó¦ĖŁĀŹĻąµČ | |
| B£® | a µć“¦Õż·“Ó¦ĖŁĀŹ±Č b µć“¦µÄ“ó | |
| C£® | d µć£Øt1 Ź±æĢ£©ŗĶ e µć£Øt2 Ź±æĢ£©“¦ n£ØN2£©²»Ķ¬ | |
| D£® | t2 Ź±æĢ£¬Õż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ |
·ÖĪö ŌŚN2£Øg£©+3H2£Øg£©?2NH3£Øg£©·“Ó¦ÖŠ£¬Ėę×Å·“Ó¦µÄ½ųŠŠ£¬·“Ó¦ĪļµÄĪļÖŹµÄĮæÖš½„¼õÉŁ£¬Éś³ÉĪļµÄĪļÖŹµÄĮæÖš½„Ōö¶ą£¬µ±“ļµ½Ę½ŗāדĢ¬Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬·“Ó¦ĪļµÄÉś³ÉĪļµÄĪļÖŹµÄĮæ²»ŌŁøı䣬ĒśĻßĪŖĖ®Ę½Ö±Ļߣ¬ŅŌ“ĖÅŠ¶ĻĢāÖŠø÷Ļī£®
½ā“š ½ā£ŗA”¢cµć·“Ó¦ĪļŗĶÉś³ÉĪļĪļÖŹµÄĮæČŌŌŚ±ä»Æ£¬Ć»ÓŠ“ļµ½Ę½ŗāדĢ¬£¬ĖłŅŌÕżÄę·“Ó¦ĖŁĀŹ²»ĻąµČ£¬¹ŹA“ķĪó£»
B”¢“Óaµćµ½bµć£¬ĒāĘųµÄĪļÖŹµÄĮæŌŚÖš½„¼õÉŁ£¬ĒāĘųµÄĪļÖŹµÄĮæÅضČŌŚÖš½„¼õÉŁ£¬ĖłŅŌÕż·“Ó¦µÄ·“Ó¦ĖŁĀŹŌŚÖš½„½µµĶ£¬¼“µćaµÄÕż·“Ó¦ĖŁĀŹ±ČµćbµÄ“󣬹ŹBÕżČ·£®
C”¢dµćŗĶeµć¶¼“¦ÓŚĘ½ŗāדĢ¬£¬n£ØN2£©²»±ä£¬¼“dµćŗĶeµćn£ØN2£©ĻąµČ£¬¹ŹC“ķĪó£»
D”¢ŌŚt2Ź±æĢ£¬øĆ·“Ó¦“¦ÓŚ»ÆŃ§Ę½ŗāדĢ¬£¬ĖłŅŌÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬¹ŹD“ķĪó£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāĶ¼ĻóĪŹĢā£¬ĢāÄæÄѶČÖŠµČ£¬×¢Ņā·ÖĪöĶ¼ĻóÖŠø÷ĪļĄķĮæµÄ±ä»ÆĒśĻߣ¬°ŃĪÕĘ½ŗāדĢ¬µÄĢŲÕ÷ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£®


 ČŹ°®Ó¢ÓļĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø
ČŹ°®Ó¢ÓļĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø ѧĻ°Źµ¼łŌ°µŲĻµĮŠ“š°ø
ѧĻ°Źµ¼łŌ°µŲĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
 Ä³Ń§ÉśæĪĶā»ī¶ÆŠ”×éĄūÓĆĶ¼ĖłŹ¾×°ÖĆ×öŹµŃé£ŗŌŚŹŌ¹Ü֊עČėijŗģÉ«ČÜŅŗ£¬¼ÓČČŹŌ¹Ü£¬ČÜŅŗŃÕÉ«Öš½„±äĒ³Ö±ÖĮĶŹÉ«£¬ĄäČ“ŗó»Öø“ŗģÉ«£¬ŌņŌČÜŅŗæÉÄÜŹĒ£Ø””””£©
Ä³Ń§ÉśæĪĶā»ī¶ÆŠ”×éĄūÓĆĶ¼ĖłŹ¾×°ÖĆ×öŹµŃé£ŗŌŚŹŌ¹Ü֊עČėijŗģÉ«ČÜŅŗ£¬¼ÓČČŹŌ¹Ü£¬ČÜŅŗŃÕÉ«Öš½„±äĒ³Ö±ÖĮĶŹÉ«£¬ĄäČ“ŗó»Öø“ŗģÉ«£¬ŌņŌČÜŅŗæÉÄÜŹĒ£Ø””””£©| A£® | ČÜÓŠSO2µÄĘ·ŗģČÜŅŗ | B£® | µĪÓŠ·ÓĢŖµÄ°±Ė®ČÜŅŗ | ||
| C£® | µĪÓŠ·ÓĢŖµÄNaOHČÜŅŗ | D£® | µĪÓŠŹÆČļµÄŃĪĖįČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 µÄøß¾ŪĪļ£¬Ę䵄ĢåÓ¦ŹĒ£Ø””””£©
µÄøß¾ŪĪļ£¬Ę䵄ĢåÓ¦ŹĒ£Ø””””£©| A£® | ¢Ł¢Ś | B£® | ¢Ł¢Ū | C£® | ¢Ü¢Ż | D£® | ¢Ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņijČÜŅŗÖŠµĪ¼ÓBaCl2ČÜŅŗ£¬ČōÓŠ°×É«³Įµķ£¬ŌŁµĪ¼Ó×ćĮæĻ”HNO3£¬Čō³Įµķ²»Čܽā£¬ŌņĖµĆ÷ŌČÜŅŗÖŠŅ»¶Øŗ¬SO42- | |
| B£® | ĻņijČÜŅŗÖŠĻȵĪ¼ÓĻõĖįŌŁµĪ¼ÓKSCNČÜŅŗ£¬ČōČÜŅŗ³öĻÖŃŖŗģÉ«ŌņĖµĆ÷ŌČÜŅŗÖŠŗ¬Fe3+ | |
| C£® | ĻņijČÜŅŗÖŠµĪ¼Ó×ćĮæĻ”HCl£¬²śÉśµÄĘųĢåÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬ŌņĖµĆ÷ŌČÜŅŗÖŠŅ»¶Øŗ¬CO32-»ņHCO3- | |
| D£® | ĻņijŃĪČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗ²¢¼ÓČČ£¬²śÉśŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶µÄĘųĢ壬ŌņŌČÜŅŗŗ¬NH4+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
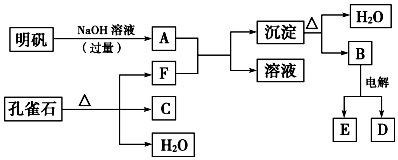
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ö÷×å ÖÜĘŚ | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | 0 |
| 2 | ¢Ł | ¢Ś | ¢Ū | |||||
| 3 | ¢Ü | ¢Ż | ¢Ž | ¢ß | ¢ą | |||
| 4 | ¢į | ¢ā |
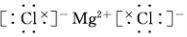 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| Ąė×Ó | æŖŹ¼³ĮµķµÄPH | ³ĮµķĶźČ«µÄPH |
| Cr3+ | 4.9 | 6.8 |
| Fe3+ | 1.5 | 4.1 |
| ĪļÖŹ | Čܽā¶Č/£Øg/110gĖ®£© | ||
| 0”ę | 40”ę | 80”ę | |
| K2SO4 | 7.4 | 14.8 | 21.4 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| ŹµŃéŠņŗÅ | “ż²āѳʷČÜŅŗµÄĢå»ż/mL | 0.1000mol/LĦ¶ūŃĪČÜŅŗµÄĢå»ż/mL | |
| µĪ¶ØĒ°æĢ¶Č | µĪ¶ØŗóæĢ¶Č | ||
| 1 | 25.00 | 0.00 | 24.98 |
| 2 | 25.00 | 1.56 | 29.30 |
| 3 | 25.00 | 1.00 | 26.02 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÖŹĮæŹżŹĒ1 | B£® | ÖŹ×ÓŹżŹĒ2 | C£® | ÖŠ×ÓŹżŹĒ2 | D£® | µē×ÓŹżŹĒ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com