
1000℃时,在恒容密封容器中发生下列反应:Na2SO4(s)+4H2(g)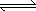 Na2S(s)+4H2O(g).
Na2S(s)+4H2O(g).
(1)该温度下,在2 L盛有1.42 g Na2SO4的密闭容器中通入H2气体,5分钟后测得固体质量为1.10 g.则5分钟内H2的平均反应速率为________.
(2)能说明该反应已达到平衡状态的是________(填序号).
a.容器内压强保持不变
b.容器内气体密度保持不变
c.c(H2)=c(H2O)
d.v正(H2)=v逆(H2O)
(3)向该容器中分别加入以下物质,对平衡的影响如何?,(填“正向移动”,“逆向移动”或“不发生移动”)①加入少量Na2SO4固体,则平衡:________②加入少量灼热的碳粉,则平衡:________
(4)若将反应后的物质溶于水,用有关离子方程式说明上述反应产物水溶液的酸碱性________,欲使该溶液中S2-浓度增大,平衡逆向移动,可加入的物质是________.
科目:高中化学 来源: 题型:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
| A | B | C | D | |
| n(CO2)/mol | 3 | 1 | 0 | 1 |
| n(H2)/mol | 2 | 1 | 0 | 1 |
| n(CO)/mol | 1 | 2 | 3 | 0.5 |
| n(H2O)/mol | 5 | 2 | 3 | 2 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年上海市高三第一次考试化学试卷 题型:填空题
1000℃时,在恒容密封容器中发生下列反应:Na2SO4(s)+4H2(g) Na2S(s)+4H2O(g)。
Na2S(s)+4H2O(g)。
(1)该温度下,在2L盛有1.42 g Na2SO4的密闭容器中通入H2气体,5分钟后测得固体质量为1.10 g。
则5分钟内H2的平均反应速率为 。
(2)能说明该反应已达到平衡状态的是____(填序号)。
a.容器内压强保持不变 b.容器内气体密度保持不变
c.c(H2)=c(H2O) d.v正(H2)=v逆(H2O)
(3)向该容器中分别加入以下物质,对平衡的影响如何?,(填“正向移动”,“逆向移动”或“不发生移动”)
①加入少量Na2SO4固体,则平衡: ②加入少量灼热的碳粉,则平衡:__
(4)若将反应后的物质溶于水,用有关离子方程式说明上述反应产物水溶液的酸碱性___ _,欲使该溶液中S2-浓度增大,平衡逆向移动,可加入的物质是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
1000℃时,在恒容密封容器中发生下列反应:Na2SO4(s)+4H2(g)![]() Na2S(s)+4H2O(g)。
Na2S(s)+4H2O(g)。
(1)该温度下,在2L盛有1.42 g Na2SO4的密闭容器中通入H2气体,5分钟后测得固体质量为1.10 g。
则5分钟内H2的平均反应速率为 。
(2)能说明该反应已达到平衡状态的是____(填序号)。
a.容器内压强保持不变 b.容器内气体密度保持不变
c.c(H2)=c(H2O) d.v正(H2)=v逆(H2O)
(3)向该容器中分别加入以下物质,对平衡的影响如何?,(填“正向移动”,“逆向移动”或“不发生移动”)
①加入少量Na2SO4固体,则平衡: ②加入少量灼热的碳粉,则平衡:__
(4)若将反应后的物质溶于水,用有关离子方程式说明上述反应产物水溶液的酸碱性___ _,欲使该溶液中S2-浓度增大,平衡逆向移动,可加入的物质是 。
查看答案和解析>>
科目:高中化学 来源:2012届上海市南汇中学高三第一次考试化学试卷 题型:填空题
1000℃时,在恒容密封容器中发生下列反应:Na2SO4(s)+4H2(g)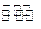 Na2S(s)+4H2O(g)。
Na2S(s)+4H2O(g)。
(1)该温度下,在2L盛有1.42 g Na2SO4的密闭容器中通入H2气体,5分钟后测得固体质量为1.10 g。
则5分钟内H2的平均反应速率为 。
(2)能说明该反应已达到平衡状态的是____(填序号)。
a.容器内压强保持不变 b.容器内气体密度保持不变
c.c(H2)=c(H2O) d.v正(H2)=v逆(H2O)
(3)向该容器中分别加入以下物质,对平衡的影响如何?,(填“正向移动”,“逆向移动”或“不发生移动”)
①加入少量Na2SO4固体,则平衡: ②加入少量灼热的碳粉,则平衡:__
(4)若将反应后的物质溶于水,用有关离子方程式说明上述反应产物水溶液的酸碱性___ _,欲使该溶液中S2-浓度增大,平衡逆向移动,可加入的物质是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com