
下列各组物质中,按熔点由低到高排列的是( )。
A.O2、I2、Hg B.CO2、Al2O3、KCl
C.Na、K、Rb D.H2S、H2Se、H2Te
科目:高中化学 来源:2014年高考化学 题型九 速率平衡型专题练习卷(解析版) 题型:选择题
一定温度下,体积为2 L的密闭容器中X、Y、Z三种气体的初始物质的量和平衡物质的量如下表:
物质 | X | Y | Z |
初始物质的量(mol) | 0.2 | 0.2 | 0 |
平衡物质的量(mol) | 0.1 | 0.05 | 0.1 |
下列说法正确的是( )
A.反应可表示为2X+3Y 2Z,其平衡常数为8 000
2Z,其平衡常数为8 000
B.增大压强使平衡向生成Z的方向移动,平衡常数增大
C.若将容器的体积压缩至1 L,则X的体积分数减小,浓度增大
D.若升高温度时,Z的浓度增大,可知温度升高时正反应速率增大,逆反应速率减小,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型一 化学社会型专题练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.2013年1月1日起,江西省正式发布环境空气质量指数(AQI),包括PM2.5、PM10、O3、CO2、SO2和NO2等6项指标
B.凡含有食品添加剂的食物对人体健康均有害,均不可食用
C.明矾水解产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒
D.将实验室的废酸液和废碱液中和后再排放符合“绿色化学”的要求
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科选修3化学训练1.2.2核外电子排布元素周期表练习卷(解析版) 题型:选择题
下列关于微粒半径的叙述中,正确的是( )。
A.金属阳离子的半径大于它的原子半径
B.金属阳离子的半径小于它的原子半径
C.非金属阴离子的半径与其原子半径相等
D.非金属阴离子的半径小于其原子半径
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科选修3化学规范训练2.4分子间作用力物质性质练习卷(解析版) 题型:填空题
如图所示每条折线表示周期表ⅣA~ⅦA族中某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是____________,b点代表的是__________。
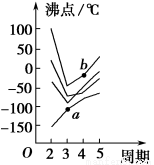
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练3章物质聚集状态物质性质练习卷(解析版) 题型:填空题
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,B、C、D同周期,A、D同主族,E和其他元素既不在同周期也不在同主族,B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。根据以上信息,回答下列问题:
(1)A和D的氢化物中,沸点较低的是________(填“A”或“D”);A和B的离子中,半径较小的是________(填离子符号)。
(2)C在元素周期表中的位置是______________。
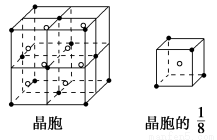
(3)A和E可形成离子化合物,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如上图所示,阳离子(用“.”表示)位于该正方体的顶点或面心,阴离子(用“。”表示)均位于小正方体的中心。该化合物的电子式是___________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练3章物质聚集状态物质性质练习卷(解析版) 题型:选择题
干冰晶体是一种面心立方结构,如图所示,即每8个CO2构成立方体,且在6个面的中心各有1个,在每个CO2周围距离为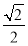 a(其中a为立方体棱长)的CO2有( )。
a(其中a为立方体棱长)的CO2有( )。
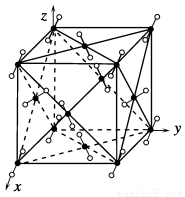
A.4个 B.8个 C.12个 D.6个
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练2章化学键分子间作用力练习卷(解析版) 题型:填空题
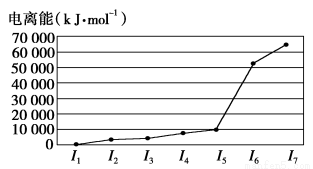
A、B、C、D、E五种元素,A元素的周期数、主族数、原子序数相同;B的基态原子核外有3种能量不同的原子轨道,且每种轨道中的电子数相同;C元素的电离能如图所示;D元素的价电子构型为nsnnpn+2;E是第4周期的过渡元素,血红蛋白中的E元素与BD形成的配位键比与D2形成的配位键强。E单质与BD形成的配合物E(BD)5,常温下呈液态,熔点为-20.5℃,沸点为103 ℃,易溶于非极性溶剂。
C元素的电离能
(1)E(BD)5晶体属于________(填晶体类型)。
(2)A元素和B元素组成的化合物分子之间________(填“能”或“不能”)形成氢键。
(3)基态E原子的电子排布式为___________________________________ 。
(4)B、C、D三种元素的电负性由大到小的顺序是________(填元素符号)。
(5)C2和B2A2的分子中根据电子云重叠的方式不同,都包含的共价键类型有________。
(6)已知原子数和电子数相同的微粒叫等电子体,等电子体的结构相似。根据
下表数据,说明BD分子比C2分子活泼的原因_____________________________。
| X—Y | X=Y | X≡Y |
BD的键能/kJ·mol-1 | 357.7 | 798.9 | 1 071.9 |
C2的键能/kJ·mol-1 | 154.8 | 418.4 | 941.7 |
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练 3.3原子晶体与分子晶体练习卷(解析版) 题型:选择题
氮化硅是一种新合成的超硬、耐磨、耐高温的材料。下列对氮化硅的叙述中,正确的是( )。
A.氮化硅是分子晶体
B.氮化硅是原子晶体
C.氮化硅是离子晶体
D.氮化硅化学式为Si4N3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com