
【题目】下列实验装置正确且能达到实验目的的是![]()
A.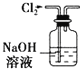 用如图所示装置除去Cl2中含有的少量HCl
用如图所示装置除去Cl2中含有的少量HCl
B.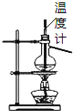 如图所示为石油分馏
如图所示为石油分馏
C.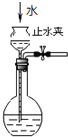 如图所示为检查装置气密性
如图所示为检查装置气密性
D.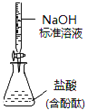 如图所示为测定未知盐酸的浓度
如图所示为测定未知盐酸的浓度
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各![]() 充入10L恒容密闭容器中,发生反应
充入10L恒容密闭容器中,发生反应![]() ,一段时间后达到平衡。反应过程中测定的数据如表:下列说法不正确的是
,一段时间后达到平衡。反应过程中测定的数据如表:下列说法不正确的是
| 2 | 4 | 7 | 9 |
|
|
|
|
|
A.反应前2min的平均速率![]()
B.其他条件不变,升高温度,反应达到新平衡前![]() 正
正![]() 逆
逆![]()
C.该温度下此反应的平衡常数![]()
D.其他条件不变,再充入![]() ,平衡时X的体积分数增大
,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤会产生![]() 、CO、
、CO、![]() 等大气污染物。燃煤脱硫的相关反应的热化学方程式如下:
等大气污染物。燃煤脱硫的相关反应的热化学方程式如下:
Ⅰ.![]()
Ⅱ.![]()
(1)一定温度下,向某恒容密闭容器中加入![]() 和1molCO,若只发生反应Ⅰ,下列能说明该反应已达到平衡状态的是______
和1molCO,若只发生反应Ⅰ,下列能说明该反应已达到平衡状态的是______![]() 填序号
填序号![]()
![]() 容器内的压强不发生变化
容器内的压强不发生变化
b.![]()
![]() 容器内气体的密度不发生变化
容器内气体的密度不发生变化
d.![]()
(2)一定温度下,体积为1L容器中加入![]() 和1molCO,若只发生反应Ⅱ,测得
和1molCO,若只发生反应Ⅱ,测得![]() 的物质的量随时间变化如图中曲线A所示:
的物质的量随时间变化如图中曲线A所示:
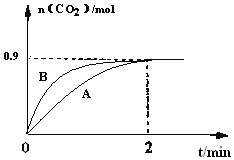
①在![]() 内的平均反应速率
内的平均反应速率![]() ______。
______。
②曲线B表示过程与曲线A相比改变的反应条件可能为______![]() 答出一条即可
答出一条即可![]() 。
。
③若要提高反应体系中![]() 的体积分数,可采取的措施为______。
的体积分数,可采取的措施为______。
(3)一定温度下,向恒容密闭容器中加入![]() 和1molCO,下列能说明反应I和反应II同时发生的是______
和1molCO,下列能说明反应I和反应II同时发生的是______![]() 填代号
填代号![]() 。
。
![]() 反应后气体能使品红褪色
反应后气体能使品红褪色
![]() 反应过程中,CO的体积分数逐渐减小
反应过程中,CO的体积分数逐渐减小
![]() 反应体系达平衡前,
反应体系达平衡前,![]() 和
和![]() 两种气体的浓度之比随时间发生变化
两种气体的浓度之比随时间发生变化
![]() 体系压强逐渐增大
体系压强逐渐增大
(4)烟道气中的![]() 和
和![]() 均是酸性氧化物,也可用氢氧化钠溶液吸收。
均是酸性氧化物,也可用氢氧化钠溶液吸收。
已知:![]() 时,碳酸和亚硫酸的电离平衡常数分别为:
时,碳酸和亚硫酸的电离平衡常数分别为:
碳酸 ![]()
亚硫酸 ![]()
①下列事实中,不能比较碳酸与亚硫酸的酸性强弱的是______![]() 填标号
填标号![]() 。
。
![]() 下,饱和碳酸溶液pH大于饱和亚硫酸溶液pH
下,饱和碳酸溶液pH大于饱和亚硫酸溶液pH
![]() 下,等浓度的
下,等浓度的![]() 溶液pH大于
溶液pH大于![]() 溶液
溶液
![]() 将
将![]() 气体通入
气体通入![]() 溶液,逸出气体通入澄清石灰水,澄清石灰水变浑浊
溶液,逸出气体通入澄清石灰水,澄清石灰水变浑浊
![]() 将
将![]() 气体通入
气体通入![]() 溶液,逸出气体通入品红溶液,品红溶液不褪色
溶液,逸出气体通入品红溶液,品红溶液不褪色
②![]() 时,氢氧化钠溶液吸收烟道气,得到
时,氢氧化钠溶液吸收烟道气,得到![]() 的吸收液,该溶液中
的吸收液,该溶液中![]() :
:![]() ______。
______。
③少量![]() 溶液和
溶液和![]() 溶液反应的离子方程式为______。
溶液反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的有机化工原料。在工业生产中可以通过乙烯和水蒸气化合生成甲醇已知:
①![]()
②![]()
③![]()
(1)请写出乙烯和水蒸气化合生成甲醇气体的热化学方程式:______。
(2)也可以将![]() 与
与 ![]() 混合,在恒容密闭容器中发生反应来制备:
混合,在恒容密闭容器中发生反应来制备:![]() ,图1是在两种投料比
,图1是在两种投料比![]() 分别为1:4和1:6时,
分别为1:4和1:6时,![]() 平衡转化率随温度变化的曲线,图2是生成的甲醇
平衡转化率随温度变化的曲线,图2是生成的甲醇![]() 过氧化氢燃料电池的工作原理示意图:
过氧化氢燃料电池的工作原理示意图:
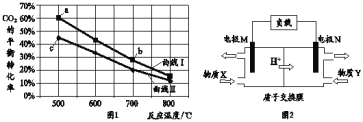
①图1中b点对应的平衡常数K值______c点对应的平衡常数K值![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() ,理由是______。
,理由是______。
②图1中a点对应的![]() 的转化率______c点对应的
的转化率______c点对应的![]() 的转化率。
的转化率。 ![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() ,
,
③图2中电极N是______![]() 填负极或正极
填负极或正极![]()
④图2中电极M的电极反应式:______。
(3)![]() 时,
时,![]() 的电离常数
的电离常数![]() ,则该温度下
,则该温度下![]() 水解反应的平衡常数
水解反应的平衡常数![]() ______,若向
______,若向![]() 溶液中加入少量的
溶液中加入少量的![]() ,则溶液中
,则溶液中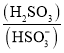 将______
将______![]() 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”![]() 。
。
(4)常温下,用NaOH溶液吸收![]() 得到
得到![]() 的
的![]() 溶液,吸收过程中水的电离平衡______
溶液,吸收过程中水的电离平衡______![]() 填“向左”、“向右”或“不”
填“向左”、“向右”或“不”![]() 移动。试计算溶液中
移动。试计算溶液中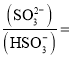 ______。
______。![]() 常温下
常温下![]() 的电离平衡常数
的电离平衡常数![]() ,
,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:
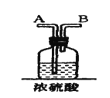
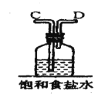
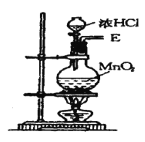
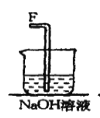
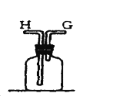
(1)该反应中生成氯气的化学方程式为:__。
(2)连接上述仪器的正确顺序是:(填各接口处的字母)E接___接___,___接___接___,___接__。___。
(3)在装置中,①饱和食盐水起的作用是__。
②浓硫酸起的作用是__。
③NaOH溶液的作用是__。
(4)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行):![]() 。三种物质的焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
。三种物质的焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
(1)写出下列物质的化学式A______,B________,C________,W________。
(2)写出A溶液与C溶液反应的离子方程式为_______________________________。
(3)向两份30 mL同浓度的A溶液中通入不同体积的W气体,得到溶液M、N。向M、N溶液中逐滴加入浓度为0.25 mol·L-1盐酸,如图所示Ⅰ和Ⅱ分别为加入V(盐酸)与产生V(W)的关系。通过计算确定A溶液的物质的量浓度为 _______________。
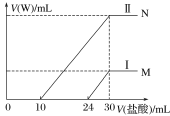
(4)M、N两溶液中相同溶质的物质的量之比为多少_______?(写出必要的文字说明和计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法不正确的是![]()
A.乙醇、乙酸和乙酸乙酯可用![]() 溶液鉴别
溶液鉴别
B.石油裂化可提高汽油的产量和质量
C.油脂中含碳碳双键,故久置后易被氧化变质
D.糖类、油脂和蛋白质均可发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是
A.异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B.2氯丁烷与NaOH乙醇溶液共热发生消去HCl分子的反应
C.甲苯在一定条件下发生硝化反应生成一硝基甲苯的反应
D.邻羟基苯甲酸与NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子中的中心原子杂化轨道的类型相同的是( )
A. SO3与SO2 B. BF3与NH3 C. BeCl2与SCl2 D. H2O与SO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com