
����Ŀ��2Na2CO33H2O2��һ�����͵���ϵƯ����ijʵ����ȤС�����������ʵ�飮
��1����ʵ���Ʊ�ʵ��ԭ����2Na2CO3+3H2O2=2Na2CO33H2O2
ʵ�鲽�裺ȡ3.5g Na2CO3����10mLH2O������0.1g�ȶ������ô���������������ȫ�ܽ��6.0mL 30%H2O2��15min�ڻ������뵽������ƿ�У�ʵ��װ����ͼ��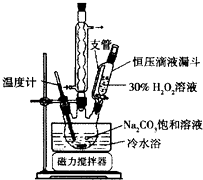
��Ӧ1Сʱ����1g�Ȼ��ƺ��ýᾧ��Ȼ����ˣ�����һ�ܺ��أ�
��װ�������������ܵ������� ��
��ʹ����ˮԡ�������� ��
�ۼ�������NaCl�����ԭ���� ��
��2Na2CO33H2O2���ֽ⣬�䷴Ӧ����ʽ�ɱ�ʾΪ ��
��2�������������ⶨȷ��ȡ����0.2000g������250mL��ƿ�У���100mLŨ��Ϊ6%��������Һ����0.0200mol/L������ر���Һ�ζ�����¼������ر���Һ���ĵ����Ϊ32.70mL���������������㹫ʽ��Q%=��40cV/m����100%[c��KMnO4����ҺŨ�ȣ�mol/L����V�����ĵ�KMnO4����Һ�����L����m������������g��]
�ٵζ��յ���ж�����Ϊ ��
�ڵζ��������漰�Ļ�ѧ����ʽ ��
�ۻ���������Ϊ ��
��3����Ʒ���ȵIJⶨΪ�˲ⶨ��Ʒ��2Na2CO33H2O2����������������˼��ַ������漰��ͬ�ķ�Ӧԭ����
����һ ��������MnO2��Ͼ��ȣ��������еμ�ˮ�������������������������м��㣮
������ ��
���𰸡�
��1��������������ֹ�¶ȹ��ߣ�H2O2�ֽ⣻���Ͳ�Ʒ���ܽ�ȣ��������ã�������������壻2��2Na2CO3?3H2O2���T4Na2CO3+6H2O+3O2��
��2����Һ����ɫ����ɫ��30s�ڲ���ɫ��5��2Na2CO3?3H2O2��+6KMnO4+19H2SO4=3K2SO4+6MnSO4+10Na2SO4+10CO2��+15O2��+34H2O��13.08%
��3�����������������Ȼ��������Ȼ��Ƶȣ���Һ��Ӧ���ˣ��������ó���������������������������������ϡ���ᷴӦ�����Ӹ���������̼����������м��㣩
���������⣺��1����װ�������������ܵ����������������������ã����Դ��ǣ������������ڹ������ⲻ�ȶ�����ʹ����ˮԡ�������Ƿ�ֹ�¶ȹ��ߣ�H2O2�ֽ⣬���Դ��ǣ���ֹ�¶ȹ��ߣ�H2O2�ֽ⣻�ۼ�������NaCl���壬���Ͳ�Ʒ���ܽ�ȣ��������ã�������������壬
���Դ��ǣ����Ͳ�Ʒ���ܽ�ȣ��������ã�������������壻��2Na2CO33H2O2���ֽ⣬����̼���ơ�������ˮ����Ӧ����ʽΪ��2��2Na2CO33H2O2���T4Na2CO3+6H2O+3O2����
���Դ��ǣ�2��2Na2CO33H2O2���T4Na2CO3+6H2O+3O2������2���ٸ�����ر���ҺΪ��ɫ������������ⷢ��������ԭ��Ӧ��������ر���Һ�ζ�2Na2CO33H2O2 �� ��ζ��յ���ж�����Ϊ��Һ����ɫ����ɫ��30s�ڲ���ɫ��
���Դ��ǣ���Һ����ɫ����ɫ��30s�ڲ���ɫ����MnԪ�صĻ��ϼ۽��ͣ�����������OԪ�ػ��ϼ����ߣ���̼����������ᷴӦ���ɶ�����̼����ζ��������漰�Ļ�ѧ����ʽΪ5��2Na2CO33H2O2��+6KMnO4+19H2SO4=3K2SO4+6MnSO4+10Na2SO4+10CO2��+15O2��+34H2O��
���Դ��ǣ�5��2Na2CO33H2O2��+6KMnO4+19H2SO4=3K2SO4+6MnSO4+10Na2SO4+10CO2��+15O2��+34H2O����0.0200mol/L������ر���Һ���ĵ����Ϊ32.70mL������0.2000g������������ΪQ%= ![]() ��100%=
��100%= ![]() ��100%=13.08%��
��100%=13.08%��
���Դ��ǣ�13.08%����3�������пɲⶨ��������ֽ����ɵ���������ⶨ̼�������ת�����ɵij���������������������ⶨ��Ʒ��2Na2CO33H2O2����������������Ϊ���������������Ȼ��������Ȼ��Ƶȣ���Һ��Ӧ���ˣ��������ó���������������������������������ϡ���ᷴӦ�����Ӹ���������̼����������м��㣩��
���Դ��ǣ����������������Ȼ��������Ȼ��Ƶȣ���Һ��Ӧ���ˣ��������ó���������������������������������ϡ���ᷴӦ�����Ӹ���������̼����������м��㣩��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���еķ�����ᴿ������ȷ����(����)
ѡ�� | Ŀ�� | ���뷽�� |
A | �������ˮ�еĵ� | �Ҵ���ȡ |
B | ��ȥCO2�е�HCl���� | ͨ��ʢ������������Һ��ϴ��ƿ |
C | ��ȥ�Ҵ��к��е�����ˮ | ������ʯ��֮��������� |
D | ������������Һ�е������� | ���������Ȼ�����Һ����� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���� �� ��
A.��ȡ����ʱ��Ҫ��ʱ��Һ©������
B.��Һ©��������ƿ��ʹ��ǰ��Ҫ��©�������þƾ�����CCl4��ȡ��ˮ�еĵⵥ��
C.����ʱ�����ʯ��Ŀ����Ϊ�˷�ֹ���У�����ʱ�¶ȼ�ˮ����Ӧ������ƿ��Һ����
D.���ε��ᴿ�����У���Һ�������м��������ᾧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ij��Һ�н���Na+��Mg2+��SO42����Cl�� �������ӣ��������Ӹ�����Ϊ��N(Na+)�UN(Mg2+)�UN(Cl��) = 4�U5�U8������N(Na+)Ϊ4a������SO42�����Ӹ���Ϊ( )
A. 2a B. 3a C. 6a D. 8a
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1.8 g H2O������ͬ��ԭ������H2SO4������Ϊ (�� ��)
A. 2.45 g B. 4.9 g C. 0.1 g D. 0.2 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������DZ�ʾ��ԭ�Ӻ������ӵ�3�ֲ�ͬ��ѧ���
�ṹʾ��ͼ | �����Ų�ʽ | �����Ų�ͼ | |
�� ԭ �� |
| 1s22s22p63s23p63d64s2 |
|
�� �� �� |
| 1s22s22p63s23p63d5 |
|
(1)��ԭ������������Ϊ ,���ڷ�����ѧ��Ӧʱ,�μӷ�Ӧ�ĵ��ӿ����� ��
(2)����ͨ���Ƚϡ�����,�ֱ�˵��3�ֲ�ͬ��ѧ�������ܷ�ӳ�����ӽṹ��Ϣ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������������Һ��ĵ�������ǿ�ڴ����������ĵ�����ǿ�ڴ�ˮ����֪Һ̬����ʶ�����ˮһ���������룻����������ƽ��(����2H2O![]() H3O++OH��)������һ���¶��¶��и��Ե����ӻ�������
H3O++OH��)������һ���¶��¶��и��Ե����ӻ�������
�ݴ˻ش���������:
(1)��������Һ̬ʱ����������ĵ��뷴Ӧ����ʽ�� ������25 ��ʱ�����ӻ�����K(H2SO4)��ˮ�����ӻ�����K(H2O) (���С������ȡ�)��
(2)�ڴ������봿�����Һ̬������У����ڵ���������Ҫ�� ;������Ϊ���Һ�в����������ֵ���ƽ��(��H2SO4��HNO3���Եĵ���ƽ�⣻�����������ǿ������)��������ˮ�������£�������з��� (д���ӷ�Ӧ����ʽ)��Ӧ����ɵġ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50g��������Ϊ��1 �� ���ʵ���Ũ��ΪC1��Ũ�����ز��������뵽VmLˮ�У�ϡ�ͺ�õ���������Ϊ��2 �� ���ʵ���Ũ��ΪC2��ϡ��Һ������˵������ȷ���ǣ� ��
A.��C1=2C2 �� ���1��2��2 �� V��50Ml
B.��C1=2C2 �� ���1��2��2 �� V��50mL
C.����1=2��2 �� ��C1��2C2 �� V=50mL
D.����1=2��2 �� ��C1��2C2 �� V��50Ml
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com