
【题目】下列说法不正确的是
A.《吕氏春秋》中“金(即铜)柔锡柔,合两柔则刚”,体现了合金硬度方面的特性
B.工业生产玻璃和水泥使用到的共同原料有![]()
C.碳纳米点是一种直径小于10nm的材料。由它作为分散质形成的分散系叫做胶体
D.天然气是一种清洁的化石燃料,作为化工原料它主要用于合成氨和甲醇
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】(1)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ/mol
③H2O(l)= H2O(g) ΔH=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式_____。
(2)已知:①Fe(s)+![]() O2(g)=FeO(s) ΔH1=272.0kJ/mol
O2(g)=FeO(s) ΔH1=272.0kJ/mol
②2Al(s)+![]() O2(g)=Al2O3(s) ΔH2=1675.7kJ/mol
O2(g)=Al2O3(s) ΔH2=1675.7kJ/mol
Al和FeO发生铝热反应的热化学方程式是________。铝热反应的反应类型_____,某同学认为,铝热反应可用于工业炼铁,你的判断是_______(填“能”或“不能”),你的理由_________。
(3)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25℃、101kPa下:
①H2(g)+![]() O2(g)=H2O(g) ΔH1=242kJ/mol
O2(g)=H2O(g) ΔH1=242kJ/mol
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) ΔH2=676kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH2=676kJ/mol
写出CO2和H2生成气态甲醇等产物的热化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数的递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
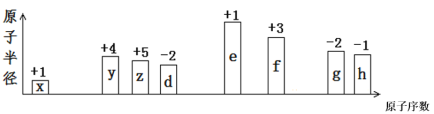
根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________________。
(2)比较d、e常见离子的半径大小(用化学式表示)___________________;
(3)z的简单氢化物与z的最高价氧化物的水化物形成的化合物中化学键类型为:_______________________。
(4)元素y的一种同位素可用于测定文物年代,这种同位素原子符号为___________。
(5)元素g与元素h相比,非金属性较强的是_________(用元素符号表示),下列表述中能证明这一事实的是_________(填序号)。
a.常温下g的单质和h的单质状态不同
b.h的氢化物比g的氢化物稳定
c.一定条件下g和h的单质都能与氢氧化钠溶液反应
d.g、h最高价氧化物对应水化物的酸性前者弱于后者
(6)x、e反应可生成离子化合物ex。
①写出化合物ex的电子式__________________。
②将少量ex投入水中,剧烈反应,得到x单质。
写出反应的化学方程式:_____________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL0.05molL-1的某稀酸H2B溶液中滴入0.1molL-1氨水,溶液中由水电离出氢离子浓度随滴入氨水体积变化如图。下列分析正确的是
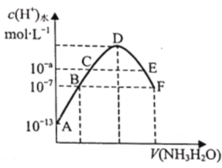
A.NaHB溶液中一定含有H2B分子
B.A、B、C三点溶液的pH逐渐减小,D、E、F三点溶液的pH逐渐增大
C.E溶液中离子浓度大小关系为c(NH4+)>c(B2-)>c(H+)>c(OH-)
D.B点溶液pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 0.1mol氯气通入水中,转移电子的数目为0.1NA
B. 常温常压下,7.8g过氧化钠含有阴离子的数目为0.2NA
C. 标准状况下,22.4LCl2与足量的铁充分反应,转移电子数为3NA
D. 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化热是指一定条件下,1mol不饱和化合物加氢时放出的热量。表中是环已烯(![]() )。环己二烯(
)。环己二烯(![]() )和苯的氢化热数据。下列说法正确的是
)和苯的氢化热数据。下列说法正确的是
化合物 |
|
|
|
氢化热 | -119.7 | -232.7 | -208.4 |
A.由氢化热数据可推测,环己二烯与![]() 的反应最剧烈
的反应最剧烈
B.环已烯、环己二烯和苯有相同的官能团
C.三种化合物中环己二烯的稳定性最强
D.上述条件下,1mol![]() 转变为
转变为![]() 时放出热量
时放出热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2 L的密闭容器内,充入0.2 mol CO与0.4 mol H2发生反应,CO(g)+2H2(g)![]() CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
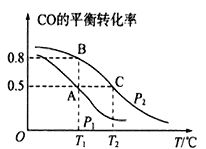
①A、B两点对应的压强大小关系是PA _______PB(填“>、<、=”)。
②在压强为P2时B、C两点的正反应速率大小关系是______________
③下列叙述能说明上述反应已达到化学平衡状态的是__________
A.H2的消耗速率是CH3OH生成速率的2倍 B.CH3OH的体积分数不再改变
C.混合气体的密度不再改变 D.CO和CH3OH的物质的量之比保持不变
(2)在压强为P1、温度为T1 ℃时,H2的平衡转化率为__________(计算出结果),再加入1.0 mol CO后重新到达平衡,则CO的转化率___________(填“增大”、“不变”或“减小”)。
(3) 在压强为P1、温度为T1 ℃时,1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.05 mol、H2:0.1mol、CH3OH:0.05mol。此时v(正)________v(逆)(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.1mol钠蒸气与2mol钠蒸气完全燃烧时,燃烧热相同
B.燃烧热是反应热的种类之一
C.在稀溶液中:H+(aq)+OH(aq)![]() H2O(l) ΔH=57.3kJ·mol1,若将含1molHNO3的稀溶液与含1molBa(OH)2的稀溶液混合,放出的热量为57.3kJ
H2O(l) ΔH=57.3kJ·mol1,若将含1molHNO3的稀溶液与含1molBa(OH)2的稀溶液混合,放出的热量为57.3kJ
D.在101kPa、25℃时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)![]() 2H2O(l) ΔH=+285.8kJ·mol1
2H2O(l) ΔH=+285.8kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃,101kPa下,lg C8H18(辛烷)(相对分子质量:114)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是( )
A. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(g);△H=-48.40kJ·mol-1
B. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1);△H=-5518kJ·mol-1
C. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1);△H=+5518kJ·mol-1
D. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1);△H=-48.40kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com