
【题目】下列说法不正确的是 ( )
A. 0.2 mol·L-1的NaHCO3溶液中:c(Na+)>c(HCO![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B. 叠氮酸(HN3)与醋酸酸性相似,NaN3水溶液中离子浓度大小顺序为c(Na+)>c(N![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
C. 常温下向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中c(NH![]() )=c(Cl-)
)=c(Cl-)
D. 常温下,等pH的CH3COONa、NaHCO3、NaClO三种溶液的浓度大小关系为c(NaClO)>c(NaHCO3)>c(CH3COONa)
【答案】D
【解析】0.2 molL﹣1的NaHCO3溶液中HCO3﹣的水解大于电离,溶液呈碱性,溶液中离子浓度大小c(Na+)>c(HCO3﹣)>c(OH﹣)>c(H+),A项正确;NaN3水溶液中叠氮酸根离子水解溶液显碱性,NaN3水溶液中离子浓度大小顺序为c(Na+)>c(N3﹣)>c(OH﹣)>c(H+),B项正确;常温下向氨水中逐滴滴入盐酸至溶液的pH=7,c(OH﹣)=c(H+),根据电荷守恒分析,c(NH4+)+c(H+)=c(Cl﹣)+c(OH﹣);则混合液中c(NH4+)=c(Cl﹣),C项正确;酸性大小为:CH3COOH>H2CO3>HClO,酸越弱酸根离子水解程度越大,常温下,等pH的CH3COONa、NaHCO3、NaClO三种溶液的浓度大小关系为c(NaClO)<c(NaHCO3)<c(CH3COONa),D项错误。


科目:高中化学 来源: 题型:
【题目】将CH3CHO(易溶于水,沸点为20.8 ℃)和CH3COOH(易溶于水,沸点为117.9 ℃)分离的最合适方法是
A. 蒸馏
B. 加入Na2CO3溶液后,通过萃取的方法分离
C. 加入烧碱溶液之后蒸馏出乙醛,再加入浓硫酸,蒸馏出乙酸
D. 和Na反应后进行分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,1mol 任何气体体积为22.4L.那么在标准状况下,700L NH3 的物质的量为________mol,全部溶解在1L水中,所得溶液的质量分数为________,如果该氨水的密度为0.85gcm﹣3 , 则氨水的体积为 ________L,物质的量浓度为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】刺囊酸具有滋肝补血、凉血止血功能,结构式如图所示。下列关于刺囊酸的说法错误的是
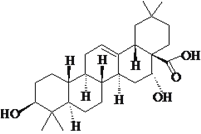
A. 所有碳原子都在同一平面上
B. 被氧气催化氧化后产物中含酮基
C. 能和NaHCO3溶液反应生成CO2
D. 能发生取代、氧化、加成等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮和硫的氧化物有多种,其中SO2和NOx都是大气污染物,对它们的研究有助于空气的净化。
(1)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K1 ΔH1<0 (Ⅰ)
NaNO3(s)+ClNO(g) K1 ΔH1<0 (Ⅰ)
2NO(g)+Cl2(g)![]() 2ClNO(g) K2 ΔH2<0 (Ⅱ)
2ClNO(g) K2 ΔH2<0 (Ⅱ)
则4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) ΔH =________(用ΔH1、ΔH2表示);平衡常数K=______(用K1、K2表示)
2NaNO3(s)+2NO(g)+Cl2(g) ΔH =________(用ΔH1、ΔH2表示);平衡常数K=______(用K1、K2表示)
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10min时反应(Ⅱ)达到平衡。测得10min内v(ClNO)=7.5×10-3molL-1min-1,NO的转化率α1=_______。其他条件保持不变,若反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2____α1(填“>”、“<”或“=”)。
(3)汽车使用乙醇汽油可减少石油的消耗,并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。NO2尾气常用NaOH溶液吸收,生成NaNO3和 NaNO2 ,已知常温下NO2-的水解常数Kh=2×10-11 molL-1。 常温下某NaNO2和HNO2混合溶液的pH=5,则混合溶液中c(NO2-)和c(HNO2)的比值为_________。
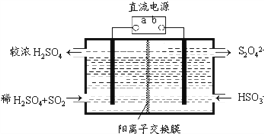
(4)利用右图所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2。阳极的电极反应式为_______________。在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体N2,同时有SO42-生成。该应的离子方程式为___________________。
(5)某研究性学习小组欲探究SO2能否与BaCl2溶液反应生成BaSO3沉淀。查阅资料得知常温下BaSO3的Ksp=5.48×10-7,饱和亚硫酸中c(SO32-) =6.3×10-8 molL-1。将0.1 mol L-1的BaCl2溶液滴入饱和亚硫酸中,_____(填“能”、“不能”)生成BaSO3沉淀,原因是_______________________________(写出推断过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)写出下列变化的文字表达式并在括号内注明反应的基本类型。
①硫在氧气中燃烧________;
②在二氧化锰的催化下加热氯酸钾制氧气________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在汽车尾气净化装置里,气体在催化剂表面吸附与释放的过程如图所示.下列说法正确的是( )
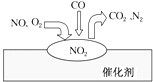
A. NO是该过程的中间产物 B. NO和O2必须在催化剂表面才能反应
C. 汽车尾气的主要污染成分包括CO2和N2 D. 汽车尾气的主要污染物是CO和NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式表达正确的是
A. 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-==2A1O2-+ H2O
B. 小苏打用于治疗胃酸过多:CO32-+2H+==CO2↑+H2O
C. 黄色的AgI悬浊液中加入Na2S溶液后变黑:2Ag++S2-=Ag2S ↓
D. 用惰性电极电解熔融氯化钠:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液X中可能含有K+、Mg2+、Al3+、AlO、SiO、CO、SO、SO中的若干种离子。某同学对该溶液进行了如下实验:

下列判断正确的是( )
A. 气体甲一定是纯净物 B. 沉淀甲是硅酸和硅酸镁的混合物
C. K+、AlO和SiO一定存在于溶液X中 D. CO和SO一定不存在于溶液X中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com