
| A. | X的氧化物的熔点比Y的氧化物的熔点低 | |
| B. | X的氧化物和Z的最高价氧化物化合的产物中有共价键和离子键 | |
| C. | 简单离子半径:W>Z>Y>X | |
| D. | Z的氢化物比W的氢化物更稳定 |
分析 短周期元素X、Y、Z和W的原子序数依次递增,且在同一周期,X的最高正价是W的最低负价的绝对值的2倍,设X、W最外层电子数分别为a、b,则a=2(8-b),且a<b<8,b-a≥3,解得:a=2,b=7;四种元素所在族的族序数之和为18,即四种元素原子的最外层电子数之和为18,则Y、Z的最外层电子数之和=18-2-7=9,则Y最外层电子数为3、Z原子最外层电子数为6,由于X和Z元素原子的原子序数比为3:4可推知,X为Mg、Y为Al、Z为S、W为Cl,据此进行解答.
解答 解:短周期元素X、Y、Z和W的原子序数依次递增,且在同一周期,X的最高正价是W的最低负价的绝对值的2倍,设X、W最外层电子数分别为a、b,则a=2(8-b),且a<b<8,b-a≥3,解得:a=2,b=7;四种元素所在族的族序数之和为18,即四种元素原子的最外层电子数之和为18,则Y、Z的最外层电子数之和=18-2-7=9,则Y最外层电子数为3、Z原子最外层电子数为6,由于X和Z元素原子的原子序数比为3:4可推知,X为Mg、Y为Al、Z为S、W为Cl,
A.X的氧化物为MgO,Y为氧化物为氧化铝,氧化镁的熔点大于氧化铝,故A错误;
B.X的最高价氧化物为MgO,Z的最高价氧化物为三氧化硫,二者化合反应生成硫酸镁,镁离子与硫酸根之间形成离子键,硫酸根中含有共价键,故B正确;
C.离子的电子层越多,离子半径越大,电子层相同时,离子的核电荷数越大,离子半径越小,则简单离子半径:Z>W>X>Y,故C错误;
D.非金属性越强,对应氢化物的稳定性越强,非金属性S(Z)<Cl(W),则Z的氢化物不如W的氢化物稳定,故D错误;
故选B.
点评 本题考查位置结构与性质关系的应用,题目难度不大,推断元素为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及逻辑推理能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 石蜡油分解产生的气体能使酸性高锰酸钾溶液褪色,说明该气体中一定含有乙烯 | |
| B. | 聚乙烯塑料中含有大量碳碳双键,容易老化,所以不能做食品包装材料 | |
| C. | 生活中很多有机物,如二糖、多糖、蛋白质、多肽都能发生水解反应 | |
| D. | 有机物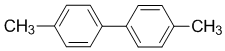 的一氯代物有4种 的一氯代物有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M、Q、R 三种元素组成的物质中只含共价键 | |
| B. | 碳元素与 R 元素形成的原子个数比为 1:1 的化合物只有 1 种 | |
| C. | X 单质常温下与 M 单质反应,生成 X2M2 | |
| D. | QMX 是形成酸雨和雾霾的原因之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用于消除H7N9病毒的漂白粉是一种强电解质 | |
| B. | 古代制盐(NaCl)有“东晒西煮”之说,是利用了复杂的物理、化学方法 | |
| C. | 铜带(镀锡)是光伏电池的电子元件,破损时不加快其腐蚀 | |
| D. | 纤维素、蛋白质和油脂均可发生水解,都属于天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自来水厂用明矾净水,用Fe2(SO4)3或ClO2均能代替明矾净水 | |
| B. | 青篙素在超临界CO2中有很强的溶解性,萃取青蒿素可用超临界CO2作萃取剂 | |
| C. | 用石灰水或MgSO4溶液喷涂在树干上均可消灭树皮上的过冬虫卵 | |
| D. | 新型材料聚碳酸酯纤维、石墨烯纤维都属于有机高分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L CC14所含的原子数为0.5 NA | |
| B. | 0.1 mol FeCl3水解生成的Fe(OH)3胶粒数为0.1 NA | |
| C. | 将lmol Cl2通人水中,HC1O、Cl-、C1O-粒子数之和为2 NA | |
| D. | 11.2 g 铁粉与足量稀硝酸反应失去电子数一定为0.6 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
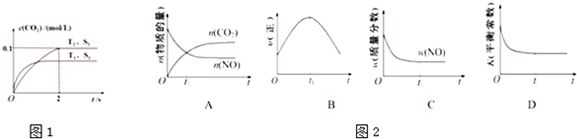
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com